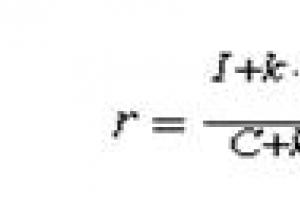Wyznacz średnią pojemność cieplną w zakresie temperatur. Pojemność cieplna jest prawdziwa, średnia, izochoryczna i izobaryczna. Wytyczne dotyczące przygotowania laboratorium
Pojemność cieplna to stosunek ilości ciepła oddanego do układu do obserwowanego w tym przypadku wzrostu temperatury (przy braku Reakcja chemiczna, przejście substancji z jednego stanu skupienia do drugiego i przy A "= 0.)
Pojemność cieplna jest zwykle obliczana na 1 g masy, wtedy nazywa się ją właściwą (J / g * K), lub na 1 mol (J / mol * K), wtedy nazywa się molową.
Wyróżnić średni i prawdziwy pojemność cieplna.
Środek pojemność cieplna to pojemność cieplna w zakresie temperatur, tj. stosunek ciepła oddanego ciału do przyrostu jego temperatury o ΔТ
PRAWDA Pojemność cieplna ciała to stosunek nieskończenie małej ilości ciepła otrzymanego przez ciało do odpowiadającego mu wzrostu jego temperatury.
Łatwo jest ustalić związek między średnią a rzeczywistą pojemnością cieplną:
podstawiając wartości Q do wyrażenia na średnią pojemność cieplną mamy:
![]()
Rzeczywista pojemność cieplna zależy od rodzaju substancji, temperatury i warunków, w których zachodzi przenoszenie ciepła do układu.
Tak więc, jeśli układ jest zamknięty w stałej objętości, tj izochoryczny mamy proces:
Jeśli system rozszerza się lub kurczy, podczas gdy ciśnienie pozostaje stałe, tj. Dla izobaryczny mamy proces:
Ale zatem ΔQ V = dU i ΔQ P = dH
C V = (∂U/∂T) v , i do P = (∂H/∂T) p
(jeśli jedna lub więcej zmiennych jest utrzymywana na stałym poziomie, podczas gdy inne się zmieniają, wówczas mówi się, że pochodne są częściowe w odniesieniu do zmieniającej się zmiennej).
Oba stosunki obowiązują dla dowolnych substancji i dowolnych stanów skupienia. Aby pokazać związek między C V i C P, konieczne jest rozróżnienie wyrażenia na entalpię H \u003d U + pV /
Dla gazu doskonałego pV=nRT
![]()
za jeden mol lub
Różnica R jest pracą izobarycznej ekspansji 1 mola gazu doskonałego przy wzroście temperatury o jedną jednostkę.
W przypadku cieczy i ciał stałych, ze względu na niewielką zmianę objętości po podgrzaniu, С P = С V
Zależność efektu cieplnego reakcji chemicznej od temperatury, równania Kirchhoffa.
Korzystając z prawa Hessa, można obliczyć efekt cieplny reakcji w temperaturze (zwykle 298 K), w której mierzy się standardowe ciepło tworzenia lub spalania wszystkich uczestników reakcji.
Częściej jednak konieczna jest znajomość efektu termicznego reakcji w różnych temperaturach.
Rozważ reakcję:
ν A A+ν B B= ν C С+ν DD D
Oznaczmy przez H entalpię uczestnika reakcji na 1 mol. Całkowitą zmianę entalpii ΔΗ (T) reakcji wyraża równanie:
ΔΗ \u003d (ν C H C + ν D H D) - (ν A H A + ν B H B); va, vb, vc, vd - współczynniki stechiometryczne. xr
Jeśli reakcja przebiega pod stałym ciśnieniem, wówczas zmiana entalpii będzie równa efektowi cieplnemu reakcji. A jeśli rozróżnimy to równanie ze względu na temperaturę, otrzymamy:
Równania dla procesu izobarycznego i izochorycznego
![]() I
I ![]()
zwany Równania Kirchhoffa(w postaci różniczkowej). Pozwalają jakościowo ocenić zależność efektu cieplnego od temperatury.
Wpływ temperatury na efekt cieplny określa znak wartości ΔС p (lub ΔС V)
Na ∆С p > 0 wartość , czyli wraz ze wzrostem temperatury zwiększa się efekt termiczny
Na ∆С str< 0 to znaczy wraz ze wzrostem temperatury efekt termiczny maleje.
Na ∆С p = 0- efekt termiczny reakcji nie zależy od temperatury
To znaczy, jak wynika z tego, ΔС p określa znak przed ΔН.
Pojemność cieplna to zdolność do pochłaniania pewnej ilości ciepła podczas ogrzewania lub oddawania go po schłodzeniu. Pojemność cieplna ciała to stosunek nieskończenie małej ilości ciepła, które ciało otrzymuje do odpowiedniego wzrostu jego wskaźników temperatury. Wartość jest mierzona w J/K. W praktyce stosuje się nieco inną wartość - ciepło właściwe.
Definicja
Co oznacza ciepło właściwe? Jest to ilość odnosząca się do pojedynczej ilości substancji. W związku z tym ilość substancji można mierzyć w metrach sześciennych, kilogramach, a nawet w molach. Od czego to zależy? W fizyce pojemność cieplna zależy bezpośrednio od jednostki ilościowej, do której się odnosi, co oznacza, że rozróżnia się molową, masową i objętościową pojemność cieplną. W branży budowlanej nie spotkasz się z pomiarami molowymi, ale z innymi – cały czas.
Co wpływa na ciepło właściwe?

Wiesz, jaka jest pojemność cieplna, ale jakie wartości wpływają na wskaźnik, nie są jeszcze jasne. Na wartość ciepła właściwego bezpośrednio wpływa kilka składników: temperatura substancji, ciśnienie i inne właściwości termodynamiczne.
Wraz ze wzrostem temperatury produktu wzrasta jego ciepło właściwe, jednak niektóre substancje różnią się całkowicie nieliniową krzywą w tej zależności. Na przykład, wraz ze wzrostem wskaźników temperatury od zera do trzydziestu siedmiu stopni, ciepło właściwe wody zaczyna spadać, a jeśli granica wynosi od trzydziestu siedmiu do stu stopni, to wskaźnik wręcz przeciwnie zwiększyć.
Warto zauważyć, że parametr zależy również od tego, jak mogą zmieniać się właściwości termodynamiczne produktu (ciśnienie, objętość itp.). Na przykład ciepło właściwe przy stabilnym ciśnieniu i przy stabilnej objętości będzie inne.
Jak obliczyć parametr?
Interesuje Cię jaka jest pojemność cieplna? Wzór obliczeniowy jest następujący: C \u003d Q / (m ΔT). Jakie są te wartości? Q to ilość ciepła, które otrzymuje produkt podczas ogrzewania (lub uwalniane przez produkt podczas chłodzenia). m to masa produktu, a ΔT to różnica między końcową i początkową temperaturą produktu. Poniżej znajduje się tabela pojemności cieplnej niektórych materiałów.

Co można powiedzieć o obliczaniu pojemności cieplnej?
Obliczenie pojemności cieplnej nie jest zadaniem łatwym, zwłaszcza jeśli stosuje się wyłącznie metody termodynamiczne, nie da się tego zrobić dokładniej. Dlatego fizycy posługują się metodami fizyki statystycznej lub znajomością mikrostruktury produktów. Jak obliczyć dla gazu? Pojemność cieplna gazu jest obliczana z obliczenia średniej energii ruchu termicznego poszczególnych cząsteczek w substancji. Ruchy cząsteczek mogą być typu translacyjnego i obrotowego, a wewnątrz cząsteczki może znajdować się cały atom lub drgania atomów. Statystyka klasyczna mówi, że dla każdego stopnia swobody ruchów obrotowych i translacyjnych istnieje wartość molowa, która jest równa R/2, a dla każdego wibracyjnego stopnia swobody wartość jest równa R. Reguła ta jest również nazywana prawo ekwipartycyjne.
W tym przypadku cząsteczka gazu jednoatomowego różni się tylko o trzy translacyjne stopnie swobody, a zatem jej pojemność cieplna powinna być równa 3R/2, co doskonale zgadza się z doświadczeniem. Każda dwuatomowa cząsteczka gazu ma trzy translacyjne, dwa obrotowe i jeden wibracyjny stopień swobody, co oznacza, że prawo ekwipartycji będzie wynosić 7R/2, a doświadczenie wykazało, że pojemność cieplna mola gazu dwuatomowego w zwykłej temperaturze wynosi 5R/ 2. Skąd taka rozbieżność w teorii? Wszystko wynika z faktu, że przy ustalaniu pojemności cieplnej konieczne będzie uwzględnienie różnych efektów kwantowych, innymi słowy wykorzystanie statystyki kwantowej. Jak widać, pojemność cieplna jest dość skomplikowanym pojęciem.
Mechanika kwantowa mówi, że każdy układ cząstek, które oscylują lub obracają się, w tym cząsteczka gazu, może mieć pewne dyskretne wartości energii. Jeżeli energia ruchu termicznego w zainstalowany system jest niewystarczająca do wzbudzenia oscylacji o wymaganej częstotliwości, to oscylacje te nie przyczyniają się do zwiększenia pojemności cieplnej układu.
W ciałach stałych ruch termiczny atomów jest słabą oscylacją wokół pewnych położeń równowagi, dotyczy to węzłów sieci krystalicznej. Atom ma trzy wibracyjne stopnie swobody i zgodnie z prawem molową pojemność cieplną ciało stałe równa się 3nR, gdzie n to liczba atomów obecnych w cząsteczce. W praktyce wartość ta jest granicą, do której dąży pojemność cieplna ciała w wysokich temperaturach. Wartość osiąga się przy normalnych zmianach temperatury w wielu pierwiastkach, dotyczy to zarówno metali, jak i prostych związków. Określa się również pojemność cieplną ołowiu i innych substancji.
Co można powiedzieć o niskich temperaturach?

Wiemy już, jaka jest pojemność cieplna, ale jeśli mówimy o niskie temperatury, to jak wtedy zostanie obliczona wartość? Jeśli mówimy o wskaźnikach niskiej temperatury, wówczas pojemność cieplna ciała stałego okazuje się proporcjonalna T 3 lub tak zwane prawo pojemności cieplnej Debye'a. Głównym kryterium odróżniania wysokich temperatur od niskich jest zwykłe porównanie ich z parametrem charakterystycznym dla danej substancji - może to być charakterystyczna temperatura Debye'a q D . Przedstawiona wartość jest wyznaczana przez widmo drgań atomów w produkcie iw dużym stopniu zależy od struktury kryształu.
W metalach elektrony przewodzące mają pewien udział w pojemności cieplnej. Ta część pojemności cieplnej jest obliczana za pomocą statystyki Fermiego-Diraca, która uwzględnia elektrony. Elektroniczna pojemność cieplna metalu, która jest proporcjonalna do zwykłej pojemności cieplnej, jest stosunkowo małą wartością i przyczynia się do pojemności cieplnej metalu tylko w temperaturach bliskich zeru absolutnemu. Wtedy pojemność cieplna sieci staje się bardzo mała i można ją pominąć.
Masowa pojemność cieplna
Ciepło właściwe dla masy to ilość ciepła, którą należy dostarczyć do masy jednostkowej substancji, aby ogrzać produkt w jednostce temperatury. Ta wartość jest oznaczona literą C i jest mierzona w dżulach podzielonych przez kilogram na kelwin - J / (kg K). To wszystko, co dotyczy pojemności cieplnej masy.
Co to jest objętościowa pojemność cieplna?

Objętościowa pojemność cieplna to określona ilość ciepła, którą należy dostarczyć do jednostki objętości produkcji, aby ją ogrzać na jednostkę temperatury. Jest mierzony w dżulach podzielonych przez metr sześcienny na kelwin lub J / (m³ K). W wielu podręcznikach budowlanych uwzględnia się ciepło właściwe dla masy podczas pracy.
Praktyczne zastosowanie pojemności cieplnej w budownictwie
Wiele materiałów ciepłochłonnych jest aktywnie wykorzystywanych do budowy ścian żaroodpornych. Jest to niezwykle ważne w przypadku domów, które charakteryzują się okresowym ogrzewaniem. Na przykład piekarnik. Produkty ciepłochłonne i zbudowane z nich ściany doskonale akumulują ciepło, magazynują je w okresach grzewczych i stopniowo oddają ciepło po wyłączeniu instalacji, pozwalając tym samym na utrzymanie akceptowalnej temperatury przez cały dzień.
Im więcej ciepła zgromadzi się w konstrukcji, tym bardziej komfortowa i stabilna będzie temperatura w pomieszczeniach.
Należy zauważyć, że zwykła cegła i beton stosowane w budownictwie mieszkaniowym mają znacznie mniejszą pojemność cieplną niż styropian. Jeśli weźmiemy ecowool, to jest on trzy razy bardziej energochłonny niż beton. Należy zauważyć, że we wzorze do obliczania pojemności cieplnej nie na próżno występuje masa. Ze względu na ogromną masę betonu czy cegły, w porównaniu z ecowoolem, pozwala na akumulację ogromnych ilości ciepła w kamiennych ścianach konstrukcji i niwelowanie wszelkich dobowych wahań temperatury. W sumie tylko niewielka masa izolacji domy szkieletowe, pomimo dobrej pojemności cieplnej, jest najsłabszym obszarem ze wszystkich technologii ramowych. Aby rozwiązać ten problem, we wszystkich domach instalowane są imponujące akumulatory ciepła. Co to jest? Są to elementy konstrukcyjne, które charakteryzują się dużą masą przy dość dobrym wskaźniku pojemności cieplnej.
Przykłady akumulatorów ciepła w życiu

Co to mogło być? Na przykład niektóre wewnętrzne ceglane ściany, duży piec lub kominek, wylewki betonowe.
Meble w każdym domu lub mieszkaniu są doskonałym akumulatorem ciepła, ponieważ sklejka, płyta wiórowa i drewno mogą tak naprawdę magazynować ciepło tylko na kilogram wagi trzy razy więcej niż osławiona cegła.
Czy są jakieś wady przechowywania termicznego? Oczywiście główną wadą tego podejścia jest konieczność zaprojektowania akumulatora ciepła na etapie tworzenia makiety. dom szkieletowy. Wynika to z faktu, że jest bardzo ciężki i trzeba będzie to wziąć pod uwagę przy tworzeniu fundamentu, a następnie wyobrazić sobie, jak ten przedmiot zostanie wkomponowany we wnętrze. Warto powiedzieć, że należy wziąć pod uwagę nie tylko masę, konieczna będzie ocena obu cech w pracy: masy i pojemności cieplnej. Na przykład, jeśli użyjesz złota o niewiarygodnej wadze dwudziestu ton na metr sześcienny jako magazynu ciepła, to produkt będzie działał tak, jak powinien, tylko o dwadzieścia trzy procent lepiej niż betonowy sześcian, który waży dwie i pół tony.
Która substancja jest najbardziej odpowiednia do magazynowania ciepła?

Najlepszym produktem na akumulator ciepła wcale nie jest beton i cegła! Miedź, brąz i żelazo dobrze sobie z tym radzą, ale są bardzo ciężkie. Dziwne, ale najlepszym akumulatorem ciepła jest woda! Ciecz ma imponującą pojemność cieplną, największą spośród dostępnych nam substancji. Większą pojemność cieplną mają tylko gazy hel (5190 J/(kg K) i wodór (14300 J/(kg K)), ale ich zastosowanie w praktyce jest problematyczne. Jeśli chcesz i potrzebujesz, zajrzyj do tabeli pojemności cieplnej substancji potrzebujesz.
POJEMNOŚĆ CIEPLNA, ilość ciepła zużytego do zmiany temperatury o 1 ° C. Według bardziej rygorystycznej definicji, pojemność cieplna-termodynamiczna. wartość określona przez wyrażenie:
Gdzie D Q - ilość ciepła przekazana do układu i spowodowana zmianą jego t-ry o D T. Stosunek różnic skończonych D Q / DT tzw. średnia pojemność cieplna, stosunek nieskończenie małych wartości d Q/dT-rzeczywista pojemność cieplna. Ponieważ d Q nie jest całkowitą różniczką funkcji stanu, pojemność cieplna zależy również od ścieżki przejścia między dwoma stanami układu. Istnieje pojemność cieplna układu jako całości (J / K), ciepło właściwe [J / (g K)], molowa pojemność cieplna [J / (mol K)]. We wszystkich poniższych wzorach stosuje się molowe pojemności cieplne.
Metody wyznaczania pojemności cieplnej poszczególnych substancji. Główny eksperymentalny metodą jest kalorymetria. Teoretyczny obliczenie pojemności cieplnej in-in przeprowadza się metodami termodynamiki statystycznej, ale jest to możliwe tylko dla stosunkowo prostych cząsteczek w stanie gazu doskonałego i dla kryształów i w obu przypadkach wymagany jest eksperyment dla obliczenie. dane dotyczące struktury wysp.
Empiryczny Metody wyznaczania pojemności cieplnej w stanie gazu doskonałego opierają się na idei addytywności wkładów poszczególnych grup atomów lub związków chemicznych. znajomości. Opublikowano obszerne tabele wkładów atomowych grup w wartość C p. Dla cieczy, oprócz metod grup addytywnych, stosuje się metody oparte na odpowiednich stanach prawa, a także na wykorzystaniu termodynamiki. cykle umożliwiające przejście do pojemności cieplnej cieczy od pojemności cieplnej gazu doskonałego przez pochodną temperaturową entalpii parowania.
Dla p-ra obliczenie pojemności cieplnej jako addytywnej funkcji pojemności cieplnej elementów jest generalnie nieprawidłowe, ponieważ nadwyżka pojemności cieplnej roztworu jest z reguły znacząca. Do jego oceny wymagane jest zaangażowanie molekularno-statystycznych. teorie roztworów (patrz Roztwory nieelektrolitów). Eksperymentalnie można wyznaczyć nadmiarową pojemność cieplną zależność od temperatury entalpia mieszania, po której można obliczyć С р р-ra.
T ciepło właściwe heterog. systemy reprezentuje naib. trudny przypadek termodynamiki. analiza. Na diagramie stanu ruchowi wzdłuż krzywej równowagi fazowej towarzyszy zmiana zarówno p, jak i T. Jeśli punkt równowagi fazowej przesuwa się podczas ogrzewania, daje to dodatek. wkład w pojemność cieplną, więc pojemność cieplna heterog. system nie jest równy sumie pojemności cieplnych jego faz składowych, ale ją przekracza. Na diagramie fazowym w przejściu z homog. stan do domeny istnienia heterog. pojemność cieplna systemu ulega skokowi (patrz Przejścia fazowe).
Wartość praktyczna badania pojemności cieplnej są ważne dla obliczeń energetycznych. bilanse procesowe w chemii reaktory i inne aparaty chemiczne. pro-va, a także wybrać optymalnie. chłodziwa. Eksperyment. pomiar pojemności cieplnej dla różnych przedziałów tp – od skrajnie niskich do wysokich – to podstawa. metoda wyznaczania termodynamiki. wejscie. Do obliczenia entalpii i entropii wyspy (w zakresie od 0 do T) stosuje się całki pojemności cieplnej:

odpowiednie efekty zostaną dodane do Krymu
Doskonałość procesów cieplnych zachodzących w cylindrze rzeczywistego silnika samochodowego oceniana jest za pomocą wskaźników indykatorowych jego rzeczywistego cyklu, natomiast doskonałość całego silnika z uwzględnieniem strat mocy na skutek tarcia i napędu mechanizmów pomocniczych, jest oceniany za pomocą skutecznych wskaźników.
Praca wykonywana przez gazy w cylindrach silnika nazywana jest pracą wskaźnika. Nazywa się pracę wskaźnika gazów w jednym cylindrze w jednym cyklu cykl pracy.
Można to określić za pomocą wykresu wskaźnikowego zbudowanego na podstawie danych obliczeń termicznych silnika.
Obszar ograniczony konturem a -c-z"-z-b-a obliczony wykres wskaźnika A T , będzie reprezentować, w odpowiedniej skali, teoretyczną wskaźnikową pracę gazów w jednym cylindrze na cykl. Rzeczywisty obszar diagramu a"-c"-c"-z"-b"-b"-r-a-a" będzie składać się z pętli górnej i dolnej. Kwadrat A D górna pętla charakteryzuje dodatnią pracę gazów na cykl. Granice tej pętli nie pokrywają się z obliczonymi ze względu na wyprzedzenie zapłonu lub wtrysk paliwa (s „-s- SS"), nienatychmiastowe spalanie paliwa (z „-z” -z"-c" i z"- z-z"„-z”) i wersji wstępnej (b"-b-b"-b").
Zmniejszenie obszaru diagramu obliczeniowego ze wskazanych powodów jest brane pod uwagę przy użyciu współczynnik kompletności diagramu :
Do silników samochodowych wartości współczynnika kompletności diagramu przyjmują wartości 0,93...0,97.
Kwadrat Jakiś dolna pętla charakteryzuje ujemną pracę wydatkowaną na skoki pompy tłoka w celu wymiany gazu w cylindrze. Zatem rzeczywista praca wskaźnika gazów w jednym cylindrze w jednym cyklu:
W praktyce wartość osiągów silnika na cykl określa średnie ciśnienie indykowane Liczba Pi, równa użytecznej pracy cyklu, odniesionej do jednostki objętości roboczej cylindra
Gdzie Wi- użyteczna praca cyklu, J (Nm); Vh– objętość robocza cylindra, m3.
Średnie ciśnienie indykatorowe - jest to warunkowo stałe ciśnienie na tłok podczas jednego skoku tłoka, które działa na równi ze wskaźnikiem pracy gazów przez cały cykl. Ciśnienie to jest wyrażone w określonej skali przez wysokość Liczba Pi prostokąt z polem A = Piekło - An io podstawie równej długości wykresu wskaźnikowego. Wartość Liczba Pi przy normalnej pracy silnika osiąga 1,2 MPa w silnikach benzynowych i 1,0 MPa w silnikach wysokoprężnych.
pożyteczna praca, wykonywana przez gazy w cylindrach silnika w jednostce czasu, nazywana jest mocą wskaźnika i jest oznaczana Liczba Pi
.
Wskaźnikowa praca gazów w jednym cylindrze dla jednego cyklu wynosi (Nm)
Rozróżnij średnią i rzeczywistą pojemność cieplną. Średnia pojemność cieplna cn to ilość ciepła zużywanego podczas ogrzewania jednostki gazu (1 kg, 1 m3, 1 mol) o 1 K od t1 do t2:
с=q/(t2-t1)
Im mniejsza różnica temperatur t2 - t1, tym bardziej wartość średniej pojemności cieplnej zbliża się do rzeczywistego c. Dlatego rzeczywista pojemność cieplna będzie miała miejsce, gdy wartość t2 - t1 zbliża się do zera.
Pojemność cieplna jest funkcją parametrów stanu - ciśnienia i temperatury, dlatego w termodynamice technicznej rozróżnia się rzeczywiste i średnie pojemności cieplne.
Pojemność cieplna gazu doskonałego zależy tylko od temperatury iz definicji można ją znaleźć tylko w zakresie temperatur. Jednak zawsze można założyć, że przedział ten jest bardzo mały w pobliżu pewnej wartości temperatury. Wtedy możemy powiedzieć, że pojemność cieplna jest określana w danej temperaturze. Ta pojemność cieplna nazywa się PRAWDA.
W literaturze przedmiotu zależność rzeczywistych pojemności cieplnych ze str I z w temperaturę podano w formie tabelarycznej i zależności analitycznych. Zależność analityczna (na przykład dla masowej pojemności cieplnej) jest zwykle przedstawiana jako wielomian:
Wówczas ilość ciepła dostarczonego w procesie w zakresie temperatur [ t1, t2] jest określona przez całkę:
W badaniu procesów termodynamicznych często określa się średnią wartość pojemności cieplnej w zakresie temperatur. Jest to stosunek ilości ciepła dostarczonego w procesie Pytanie 12 do końcowej różnicy temperatur:
Wtedy, jeśli podano zależność rzeczywistej pojemności cieplnej od temperatury, zgodnie z (2):
Często w literaturze przedmiotu podawane są wartości średnich pojemności cieplnych ze str I z w dla zakresu temperatur od 0 zanim t o C. Podobnie jak prawdziwe, są one przedstawione w formie tabel i funkcji:
Podczas zastępowania wartości temperatury T ten wzór zostanie użyty do znalezienia średniej pojemności cieplnej w zakresie temperatur [ 0.t]. Aby znaleźć średnią pojemność cieplną w dowolnym przedziale [ t1, t2], korzystając z zależności (4), należy znaleźć ilość ciepła Pytanie 12 stosowane w systemie w tym zakresie temperatur. W oparciu o regułę znaną z matematyki całkę w równaniu (2) można podzielić na następujące całki:
Następnie żądaną wartość średniej pojemności cieplnej można znaleźć za pomocą wzoru (3).