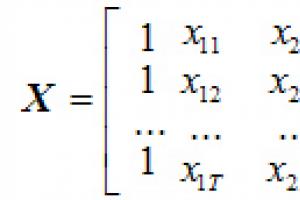تركيب المرحلة الصلبة. هيكل الببتيدات. تفاعلات تكوين الرابطة الببتيدية
يمكن تنفيذ التوليف التوافقي ليس فقط في المحلول (تخليق الطور السائل)، ولكن أيضًا على سطح الطور الخامل كيميائيًا. في هذه الحالة، يتم "خياطة" المادة البادئة الأولى كيميائيًا إلى المجموعات الوظيفية الموجودة على سطح حامل البوليمر (غالبًا ما يتم استخدام رابطة إستر أو أميد) ومعالجتها بمحلول المادة البادئة الثانية، التي يتم أخذها في فائض كبير حتى يكتمل التفاعل. هناك راحة معينة في هذا الشكل من التفاعل، حيث يتم تسهيل تقنية عزل المنتجات: يتم ببساطة ترشيح البوليمر (عادة على شكل حبيبات)، وغسله جيدًا من بقايا الكاشف الثاني، ويتم إزالة المركب المستهدف. المنشق كيميائيا منه.
في الكيمياء العضوية، لا يوجد تفاعل واحد يوفر عمليًا عوائد كمية للمنتجات المستهدفة في أي حال. ويبدو أن الاستثناء الوحيد هو الاحتراق الكامل للمواد العضوية في الأكسجين درجة حرارة عاليةإلى CO 2 وH 2 O. ولذلك، فإن تنقية المنتج المستهدف هي دائمًا مهمة لا غنى عنها، وغالبًا ما تكون المهمة الأكثر صعوبة واستهلاكًا للوقت. مهمة صعبة بشكل خاص هي عزل منتجات تخليق الببتيد، على سبيل المثال، فصل خليط معقد من الببتيدات. لذلك، في تخليق الببتيد، أصبحت طريقة التوليف على ركيزة بوليمر صلبة، التي طورها آر بي ميريفيلد في أوائل الستينيات، مستخدمة على نطاق واسع.
حامل البوليمر في طريقة ميريفيلد عبارة عن بوليسترين حبيبي متشابك يحتوي على مجموعات كلورو ميثيل في حلقات البنزين، وهي روابط تربط الدعامة ببقايا الحمض الأميني الأول للبولي ببتيد. تعمل هذه المجموعات على تحويل البوليمر إلى نظير وظيفي لكلوريد البنزيل وتمنحه القدرة على تكوين روابط إستر بسهولة عند التفاعل مع أنيونات الكربوكسيل. يؤدي تكثيف هذا الراتنج مع الأحماض الأمينية المحمية بـ N إلى تكوين استرات البنزيل المقابلة. إزالة الحماية N من يعطي مشتق محمي C للحمض الأميني الأول المرتبط تساهميًا بالبوليمر. يؤدي التحلل الأميني للمجموعة الأمينية المحررة مع مشتق محمي N من الحمض الأميني الثاني، متبوعًا بإزالة الحماية N، إلى مشتق ثنائي الببتيد مماثل مرتبط أيضًا بالبوليمر:
يمكن، من حيث المبدأ، تكرار مثل هذه الدورة المكونة من مرحلتين (إزالة الحماية - التحلل الأميني) عدة مرات حسب الحاجة لبناء سلسلة بولي ببتيد بطول معين.
كان التطوير الإضافي لأفكار Merifield يهدف في المقام الأول إلى إيجاد وإنشاء أفكار جديدة مواد البوليمرللركائز، وتطوير طرق لفصل المنتجات وإنشاء مرافق آلية للدورة الكاملة لتخليق البولي ببتيد
وقد تم إثبات فعالية طريقة ميريفيلد من خلال التوليف الناجح لعدد من الببتيدات الطبيعية، وخاصة الأنسولين. وقد تم توضيح مزاياه بشكل خاص من خلال مثال تخليق إنزيم الريبونوكلياز. لذلك، على سبيل المثال، وعلى حساب جهود كبيرة، وعلى مدار عدة سنوات، قام هيرشمان و22 موظفًا بتخليق إنزيم ريبونوكلياز (124 من بقايا الأحماض الأمينية) باستخدام طرق الطور السائل التقليدية. وفي الوقت نفسه تقريبًا، تم الحصول على نفس البروتين عن طريق تخليق الطور الصلب الآلي. وفي الحالة الثانية التوليف الذي يتضمن إجمالي 11.931 عملية مختلفة منها 369 التفاعلات الكيميائيةتم الانتهاء منه من قبل اثنين من المشاركين (جات وميريفيلد) في بضعة أشهر فقط.
كانت أفكار ميريفيلد بمثابة الأساس للخلق أساليب مختلفةالتوليف التوافقي لمكتبات البوليببتيدات ذات الهياكل المختلفة.
لذلك، في عام 1982، تم اقتراح استراتيجية أصلية للتوليف المتوازي متعدد المراحل للببتيدات في الطور الصلب، والمعروفة باسم "طريقة الانقسام" ( ينقسم- التقسيم والفصل) أو طريقة "الخلط والتقسيم" (الشكل 3). جوهرها هو على النحو التالي. لنفترض أنه من ثلاثة أحماض أمينية (A وB وC) تحتاج إلى الحصول على جميع التركيبات الممكنة من ثلاثي الببتيدات. للقيام بذلك، يتم تقسيم حبيبات حامل البوليمر الصلب (P) إلى ثلاثة أجزاء متساوية ومعالجتها بمحلول أحد الأحماض الأمينية. في هذه الحالة، ترتبط جميع الأحماض الأمينية كيميائيًا بسطح البوليمر بواسطة إحدى مجموعاتها الوظيفية. يتم خلط البوليمرات التي تم الحصول عليها من ثلاث درجات جيدًا، ويتم تقسيم الخليط مرة أخرى إلى ثلاثة أجزاء. ثم تتم معالجة كل جزء، يحتوي على جميع الأحماض الأمينية الثلاثة بكميات متساوية، مرة أخرى باستخدام واحد من نفس الأحماض الأمينية الثلاثة ويتم الحصول على تسعة ثنائيات الببتيد (ثلاثة مخاليط من ثلاثة منتجات لكل منها). خلط آخر، تقسيم إلى ثلاثة أجزاء متساوية ومعالجة بالأحماض الأمينية يعطي 27 ثلاثي الببتيد المطلوب (ثلاثة مخاليط من تسعة منتجات) في تسع مراحل فقط، في حين أن الحصول عليها بشكل منفصل يتطلب تركيب 27 × 3 = 81 مرحلة.
تعد تقنية الطور الصلب أو تقنية الطور الصلب، والتي تسمى غالبًا بالسيراميك، هي الأكثر شيوعًا في إنتاج المواد غير العضوية لمختلف فروع العلوم والصناعة. وتشمل هذه الوقود النووي، والمواد اللازمة لتكنولوجيا الفضاء، والإلكترونيات الراديوية، والأجهزة، والمحفزات، والحراريات، والموصلات الفائقة ذات درجة الحرارة العالية، وأشباه الموصلات، والمواد الحديدية والكهرضغطية، والمغناطيس، والمواد المركبة المختلفة، وغيرها الكثير.
يعتمد تخليق الطور الصلب على تفاعلات كيميائية يكون فيها أحد المواد المتفاعلة على الأقل على شكل مادة صلبة. تسمى هذه التفاعلات بالطور غير المتجانس أو الصلب. يتكون تفاعل المرحلة الصلبة، على عكس التفاعلات في الوسط السائل أو الغازي، من عمليتين أساسيتين: من التفاعل الكيميائي نفسه ونقل المادة إلى منطقة التفاعل.
تتميز تفاعلات الحالة الصلبة التي تتضمن مكونات بلورية بالحركة المحدودة لذراتها أو أيوناتها واعتمادها المعقد على العديد من العوامل. وتشمل هذه مثل التركيب الكيميائي والتفاعل المرتبط بالمواد الصلبة المتفاعلة، وطبيعة العيوب وتركيزها، وحالة السطح ومورفولوجية منطقة التفاعل، ومنطقة التلامس للكواشف المتفاعلة، والتنشيط الميكانيكي الكيميائي الأولي، وعدد من آحرون. كل ما سبق يحدد مدى تعقيد آليات التفاعلات غير المتجانسة. تعتمد دراسة التفاعلات غير المتجانسة على كيمياء الحالة الصلبة، والفيزياء الكيميائية، والكيمياء الفيزيائية لأسطح المواد الصلبة، وعلى قوانين الديناميكا الحرارية والحركية.
في كثير من الأحيان، يتم الحكم على آلية تفاعلات الحالة الصلبة فقط على أساس أن البيانات التجريبية حول درجة التفاعل كدالة للوقت يمكن وصفها بشكل أفضل من خلال أي نموذج حركي معين والمعادلة الحركية المقابلة. هذا النهج يمكن أن يؤدي إلى استنتاجات غير صحيحة.
تحتوي العمليات في المواد الصلبة على عدد من الاختلافات المهمة عن العمليات في السوائل أو الغازات. ترتبط هذه الاختلافات، في المقام الأول، بمعدل انتشار أقل بشكل ملحوظ (بعدة مراتب من حيث الحجم) في المواد الصلبة، مما يمنع متوسط تركيز المكونات في النظام، وبالتالي يؤدي إلى التوطين المكاني للعمليات التي تحدث. يؤدي التوطين المكاني بدوره إلى حقيقة أن كلا من المعدل المحدد للعملية (أو معامل الانتشار) وهندسة منطقة التفاعل يساهمان في الحركية الملحوظة للعمليات. تسمى هذه الميزات لعمليات الطور الصلب التي تحددها العوامل الهندسية بالكيمياء الطوبوغرافية. بالإضافة إلى ذلك، نظرًا لأن التحويلات قيد المناقشة موضعية مكانيًا، فيمكن تحديد معدلها من خلال العمليات نفسها عند حدود الطور (التحكم في التفاعل) ومعدل توريد أي من المكونات إلى هذه الواجهة أو إزالة المنتج ( ق) (التحكم في الانتشار). ويمكن تحديد هذه الحالات الخاصة بالأنظمة البسيطة، التي تتوافر لها افتراضات النموذج، تجريبيا من خلال شكل الاعتماد الزمني لدرجة التحويل. ترتبط ميزة أخرى لتحولات الطور في المواد الصلبة بحقيقة أن تكوين نواة طور جديدة في مصفوفة صلبة يتسبب في ظهور ضغوط مرنة في الأخيرة، والتي يجب في بعض الحالات أن تؤخذ في الاعتبار عند النظر في الديناميكا الحرارية من هذه التحولات.
هناك عدد كبير من العوامل التي تؤثر على حركية عمليات الطور الصلب والبنية المجهرية للمواد التي يتم الحصول عليها بهذه الطريقة تحدد أيضًا تعدد أنواع تصنيف هذه العمليات. وبالتالي، مع الأخذ في الاعتبار استقرار النظام فيما يتعلق بالتقلبات بمختلف أنواعها، غير المتجانسة (في حالة الأنظمة المستقرة للتقلبات الصغيرة في الحجم المشغول وغير المستقرة للتقلبات الكبيرة) والمتجانسة (في حالة الأنظمة غير المستقرة) لتقلبات صغيرة) تتميز العمليات. بالنسبة للعمليات غير المتجانسة، على سبيل المثال، يمكن الاستشهاد بالتحولات التي تتم وفقًا لآلية تكوين ونمو النوى، وبالنسبة للعمليات المتجانسة، وبعض التحولات في اضطراب النظام والتحلل الشوكي للمحاليل الصلبة.
من الضروري التمييز بين النواة غير المتجانسة والمتجانسة والعمليات غير المتجانسة والمتجانسة في حالة العمليات غير المتجانسة. تشير النواة غير المتجانسة إلى تكوين النوى على العيوب الهيكلية (بما في ذلك العيوب النقطية والخلع وحدود الطور)؛ نواة متجانسة - تكوين نوى في حجم خالٍ من العيوب من الطور الصلب.
عند تحليل ناتج تحول الطور الصلب، يمكن التمييز بين النوى أحادية الطور والنواة متعددة الأطوار. في حالة النوى متعددة الأطوار، يكون ناتج العملية عبارة عن مستعمرة متعددة الأطوار ذات بنية مجهرية مميزة تحددها الطاقة السطحية لحدود المراحل المشكلة؛ تسمى العمليات من هذا النوع متقطعة، على عكس العمليات المستمرة في حالة تكوين ونمو النوى أحادية الطور.
هناك طريقة أخرى لتصنيف تحولات الطور الصلب تعتمد على مقارنة تكوين الطور الأولي وتكوين منتج التفاعل. إذا تزامنت، فإنها تتحدث عن عمليات خالية من الانتشار، وإذا تغير التكوين، فإنها تتحدث عن الانتشار. علاوة على ذلك، من المفيد التمييز عن العمليات غير الانتشارية العمليات التعاونية (على سبيل المثال، التحول المارتنسيتي) التي تحدث عن طريق إزاحة طفيفة متزامنة للذرات في حجم كبير من المرحلة الأولية.
يمكن أن تختلف تحولات الطور غير المنتشر في نوع خصائصها الديناميكية الحرارية المتغيرة أثناء العملية.
التحولات من النوع الأول هي العمليات التي يحدث فيها تغير في مشتقات الجهد الكيميائي بالنسبة لدرجة الحرارة أو الضغط. وهذا يعني حدوث تغيير مفاجئ أثناء المرحلة الانتقالية لمعلمات الديناميكا الحرارية مثل الإنتروبيا والحجم والمحتوى الحراري والطاقة الداخلية. أثناء التحولات من النوع الثاني، لا تتغير المشتقات الأولى للجهد الكيميائي بالنسبة للمعاملات المكثفة، ولكن تتغير المشتقات ذات الرتب الأعلى (بدءًا من الثاني). في هذه العمليات، مع الإنتروبيا المستمرة وحجم النظام، هناك تغيير مفاجئ في الكميات المعبر عنها بالمشتقات الثانية لطاقة جيبس: السعة الحرارية، ومعامل التمدد الحراري، والانضغاطية، وما إلى ذلك.
تفاعلات الطور الصلب بين مرحلتين (من غير المحتمل حدوث اتصالات بين ثلاث أطوار أو أكثر، ويمكن تمثيل العمليات المقابلة كمجموعات من عدة تفاعلات ثنائية الطور) هي عمليات انتشار ويمكن أن تكون إما غير متجانسة أو متجانسة، مع كل من النواة غير المتجانسة والمتجانسة . من الممكن إجراء عمليات وعمليات متجانسة مع نواة متجانسة في مثل هذه التفاعلات، على سبيل المثال، في حالة تكوين محلول صلب شبه مستقر مع تحلله اللاحق (ما يسمى بالتفاعلات الداخلية). مثال على هذه العمليات يمكن أن يكون الأكسدة الداخلية.
شرط التوازن الديناميكي الحراري في تحول الحالة الصلبة، كما هو الحال في أي تحول كيميائي آخر، هو تساوي الإمكانات الكيميائية للمكونات في المواد الأولية ومنتجات التفاعل. في التفاعل بين مرحلتين صلبتين، يمكن تحقيق المساواة المشار إليها في الإمكانات الكيميائية طرق مختلفة: 1) إعادة توزيع المكونات في المراحل الأولية مع تشكيل المحاليل الصلبة؛ 2) تكوين مراحل جديدة ذات بنية بلورية مختلفة (والتي، في الواقع، تسمى عادة تفاعل الطور الصلب)، وبما أن الإمكانات الكيميائية للمكون في مراحل مختلفة من نظام متعدد الأطوار لا تعتمد على كمية في كل مرحلة، لا يمكن تحقيق التوازن إلا عندما التحول الكاملالمراحل الأولية. يتم الحصول على المعلومات الأكثر موثوقية حول آلية تفاعلات الطور الصلب من خلال الاستخدام المعقد، مما يجعل من الممكن مراقبة العديد من معلمات نظام التفاعل في وقت واحد، بما في ذلك تكوين الطور، والتأثيرات الحرارية، وتغيرات الكتلة، والمزيد.
تم اقتراح النظرية الديناميكية الحرارية لتفاعلات الحالة الصلبة بواسطة فاغنر وتم تطويرها بواسطة شمالزريد باستخدام مثال تفاعلات الإضافة.
حتى الآن، لا يوجد تصنيف موحد لمجموعة واسعة من التفاعلات غير المتجانسة. ويرجع ذلك إلى صعوبة اختيار معيار كأساس لمثل هذا التصنيف العالمي. وفقًا للمعايير الكيميائية، يتم تقسيم التفاعلات إلى تفاعلات الأكسدة، والاختزال، والتحلل، والجمع، والتبادل، وما إلى ذلك. جنبًا إلى جنب مع المعيار المحدد، يتم استخدامه على نطاق واسع كمعيار رئيسي للحالة الفيزيائية للكواشف:
السمة المميزة لجميع التفاعلات غير المتجانسة هي الوجود والتوطين عند حدود الطور لمنطقة التفاعل. منطقة التفاعل، كقاعدة عامة، ذات سماكة صغيرة تفصل بين منطقتين من الفضاء تشغلهما مواد ذات تركيب مختلف ومع خصائص مختلفة. تنقسم أسباب تكوين منطقة التفاعل عادة إلى مجموعتين: البطء النسبي لعمليات الانتشار والأسباب الكيميائية. ترجع المجموعة الأخيرة إلى التفاعلية العالية للذرات أو الجزيئات الموجودة على سطح الكاشف الصلب أو على السطح البيني بين مرحلتين موجودتين. من المعروف أن سطح المادة الصلبة أو السائلة له خصائص تختلف عن الخصائص السائبة للعينة المدمجة. وهذا يجعل خصائص الواجهة محددة. وهنا تتم إعادة ترتيب كبيرة للتعبئة البلورية، وتقل الضغوط بين الشبكتين البلوريتين، ويتغير التركيب الكيميائي.
نظرًا لأن نقل الكتلة يتم عن طريق الانتشار، وتعتمد حركة انتشار الجزيئات الصلبة على عيب هيكلها، فمن الممكن توقع تأثير كبير للعيوب على آلية وحركية تفاعلات الطور الصلب. تسبق هذه المرحلة المرحلة الكيميائية لتحويل المواد المتفاعلة في الواجهة البينية. وبالتالي، يتم تحديد حركية التفاعلات غير المتجانسة من خلال طبيعة مسار التفاعل الكيميائي نفسه وطريقة توصيل المادة إلى منطقة التفاعل. وفقا لما ورد أعلاه، فإن معدل التفاعل سيكون محدودا بالمرحلة الكيميائية (الحركية الكيميائية) أو الانتشار (حركية الانتشار). وقد لوحظت مثل هذه الظاهرة في الواقع.
وفقًا لفاغنر، يتم الانتشار وبالتالي التفاعل في المواد الصلبة بشكل أساسي بسبب حركة الأيونات والإلكترونات، بسبب حالة عدم التوازن في الشبكة. تتحرك أيونات مختلفة من الشبكة بسرعات مختلفة. على وجه الخصوص، فإن حركة الأنيونات في الغالبية العظمى من الحالات تكون ضئيلة مقارنة بحركة الكاتيونات. لذلك، يتم الانتشار وبالتالي التفاعل في المواد الصلبة بسبب حركة الكاتيونات. في هذه الحالة، يمكن أن يسير انتشار الكاتيونات المتباينة في نفس الاتجاه أو تجاه بعضها البعض. في حالة الكاتيونات المشحونة بشكل مختلف، يتم الحفاظ على الحياد الإلكتروني للنظام بسبب حركة الإلكترونات. بسبب الاختلاف في معدلات حركة الكاتيونات المشحونة بشكل مختلف، ينشأ جهد كهربائي في النظام. ونتيجة لذلك، ينخفض معدل حركة الأيونات الأكثر قدرة على الحركة، وعلى العكس من ذلك، بالنسبة للأيونات الأقل قدرة على الحركة؟ يزيد. وبالتالي، فإن الإمكانات الكهربائية الناتجة تنظم معدلات انتشار الأيونات. يمكن حساب الأخير والمعدل الذي يحدده لعملية تحويل الحالة الصلبة بأكملها على أساس الموصلية الإلكترونية وأرقام النقل. من الواضح أن الانتشار الموجه للأيونات ممكن فقط في الحقل الكهربائيأو إذا كان هناك تدرج تركيز في النظام.
في تخليق المواد في الحالة الصلبة، غالبًا ما يكون من الضروري التحكم ليس فقط في التركيب الكيميائي (العنصري والمرحلة) للمنتج الناتج، ولكن أيضًا تنظيمه الهيكلي المجهري. ويرجع ذلك إلى الاعتماد القوي لكل من الخصائص الكيميائية (على سبيل المثال، النشاط في تفاعلات الطور الصلب) والعديد من الخصائص الفيزيائية (المغناطيسية والكهربائية والضوئية وما إلى ذلك) على خصائص التنظيم الهيكلي للمادة الصلبة على مستويات هرمية مختلفة. يتضمن أول هذه المستويات التركيب العنصري للمادة الصلبة وطريقة الترتيب المتبادل لذرات العناصر في الفضاء - التركيب البلوري (أو ميزات أقرب بيئة تنسيق للذرات في المواد الصلبة غير المتبلورة)، وكذلك التركيب و تركيز عيوب النقطة. باعتباره المستوى التالي من بنية الجسم الصلب، يمكننا النظر في توزيع العيوب الممتدة في البلورة، والذي يحدد أحجام المناطق التي (تم تصحيحها لوجود عيوب نقطية) لوحظ فيها التماثل الانتقالي في ترتيب الذرات . يمكن اعتبار مثل هذه المناطق بلورات دقيقة مثالية وتسمى مناطق التشتت المتماسك. عند الحديث عن مناطق التشتت المتماسك، يجب أن نتذكر أنها، في الحالة العامة، لا تعادل الجسيمات المدمجة التي تشكل مادة صلبة الطور، والتي قد تحتوي على عدد كبير من العيوب الممتدة، وبالتالي مناطق متماسكة نثر. عادة ما يتم ملاحظة تزامن مناطق التشتت المتماسك مع الجسيمات (والتي تسمى في هذه الحالة المجال الفردي) فقط لأحجام صغيرة بما فيه الكفاية (أقل من 100 نانومتر) للأخيرة. يمكن ربط المستويات الهيكلية اللاحقة بشكل وحجم الجزيئات التي تشكل المسحوق أو المادة الخزفية، وتجميعها، وتجميع الركام الأولي، وما إلى ذلك.
التطبيقات المختلفة لمواد الطور الصلب لها متطلبات مختلفة ومتضاربة في كثير من الأحيان للخصائص الهيكلية المذكورة أعلاه، وبالتالي تتطلب طرقًا تركيبية مختلفة. لذلك، من الأصح الحديث عن طرق التوليف ليس للمواد ذات الطور الصلب، ولكن للمواد ذات الطور الصلب، وفي كل حالة، اختر طريقة التوليف مع الأخذ في الاعتبار مجال التطبيق اللاحق للمنتج الناتج.
في الحالة العامة، يمكن تصنيف طرق تصنيع المواد ذات الطور الصلب وفقًا لبعدها عن ظروف التوازن الديناميكي الحراري لتدفق العمليات الكيميائية المستخدمة. وفقًا للقوانين العامة، في ظل الظروف المقابلة لحالة بعيدة قدر الإمكان عن التوازن، لوحظ وجود فائض كبير في معدل النواة مقارنة بمعدل نمو النوى المشكلة، مما يؤدي بوضوح إلى الحصول على المنتج الأكثر تشتتًا. في حالة تنفيذ العملية بالقرب من التوازن الديناميكي الحراري، يحدث نمو النوى التي تم تشكيلها بالفعل بشكل أسرع من تكوين نوى جديدة، وهذا بدوره يجعل من الممكن الحصول على مواد ذات حبيبات خشنة (في الحالة المقيدة، أحادية البلورة). يتم أيضًا تحديد معدل نمو البلورات إلى حد كبير من خلال تركيز العيوب الممتدة (غير المتوازنة) فيها.
يعتمد تخليق الطور الصلب على حقيقة أن الرابط الأول من قليل القسيم المستقبلي مرتبط تساهميًا بمجموعة "المرساة" H. ويتم تنفيذ تمديد السلسلة باستخدام المونومرات المحمية القياسية وفقًا للمخططات المعتادة المستخدمة للتوليف في المحاليل. ليستنتج. مرحلة التوليف. يتم فصل القلة من N. وتنقيتها بالطرق المناسبة. يتم استخدام تخليق المرحلة الصلبة بشكل رئيسي. للحصول على عديدات الببتيد وأليغنوكليوتيدات وقليلة السكاريد.
أثناء تركيب الببتيدات مثل N. naib. يتم استخدام بوليمر مشترك من الستايرين و1-2% ديفينيل بنزين على نطاق واسع، ويتم تعديله عن طريق إدخال مجموعة تثبيت كلوريد ثنائي ميثوكسي بنزيل لربط أول حمض أميني (مع مجموعة N H 2 محمية) عند الطرف C، على سبيل المثال:
بعد إزالة المجموعة الواقية N، يتم تمديد سلسلة البولي ببتيد بواسطة الطرق القياسية لتخليق الببتيد في المحلول (انظر الببتيدات). كعوامل تكثيف، نايب. غالبًا ما يتم استخدام الكاربوديميدات أو يتم تحويل الأحماض الأمينية مبدئيًا إلى منشط. الأثيرات.
في تركيب أليغنوكليوتيدات، يتم استخدام الزجاج كبير المسام أو هلام السيليكا كأحماض نووية. مجموعة المرساة هي مجموعة كربوكسيل، مفصولة عن N. spec. "الساق"، على سبيل المثال:

ب- البيورين أو قاعدة بيريميديك
في المرحلة الأولى، يتم ربط النيوكليوسيد بالحامل عند مجموعة 3 "-هيدروكسيل من ديوكسيريبوز، حيث تكون مجموعة الهيدروكسيل في الموضع 5" محمية بواسطة مجموعة ثنائي ميثوكسيتريتيل (CH 3 OS 6 H 4) 2 (C 6 H 5) ج (دمتر)؛ يمكن قياس كمية الأخير بعد انفصاله بسهولة باستخدام القياس الطيفي، والذي يعمل ككمية. خاصية تحميل الناقل وتسمح لك بتقييم الإنتاج في المراحل اللاحقة من بناء سلسلة قليل النوكليوتيد. بعد إزالة مجموعة DMTr، يتم تجميع السلسلة باستخدام الفوسفيتاميدات (fl. I; M. Kaposers, 1980) أو الفوسفونات (الهيدروفسفونات) (II; R. Stremberg, 1986):

لتنفيذ تخليق المرحلة الصلبة، مطلوب إنتاجية عالية (على مستوى 96-99٪) في كل مرحلة من مراحل المنطقة، وكذلك طرق فعالةتنقية وعزل المواد المركبة. روابط.
إن استخدام الطور الصلب يجعل من الممكن تبسيط وتسريع كل مرحلة من مراحل نمو سلسلة القلة بشكل كبير، حيث يتم فصل المكونات الزائدة وعوامل التكثيف والمنتجات الثانوية في المحلول عن طريق تصفية التفاعلات. الخلطات والغسيل N. بمجموعة مناسبة من المحاليل. وبالتالي، فإن عملية تجميع سلسلة القلة تنقسم إلى عدد من العمليات القياسية: إزالة انسداد الطرف المتنامي من السلسلة، وتحديد جرعات المونومر المحمي التالي وعامل التكثيف، وتغذية العمود N. بهذا الخليط للوقت المحسوب، والغسيل. خارج N. مع مذيب مناسب. دورة بناء وصلة أحادية م.ب. الآلي.
في قلب الأوتوماتيكية حفلة موسيقية. موالفة الأكاذيب المشتركة مخطط الرسم البياني(انظر الشكل). عديد تختلف نماذج المركب في تصميم الأعمدة وعددها، وطريقة توريد الكواشف والمذيبات، وما إلى ذلك. ويتم التحكم والبرمجة باستخدام جهاز كمبيوتر مدمج أو بعيد.

رسم تخطيطي للجهاز التلقائي. حفلة موسيقية. المُركِّبات (يُشار إلى خط التحكم الكهربائي بخط منقط): 1 - خط إمداد المونومرات (M 1 , M n) وعامل التكثيف (KA) ؛ إمداد بخطين من الكواشف (على سبيل المثال، العوامل المؤكسدة، عوامل الأسيلة، to-t، إلخ.) والمذيبات p (P 1، P n)؛ 3 - تبديل الصمامات. 4-عمود مع الوسائط ومجهز بالتوزيع. صمام؛ 5-القياس الضوئي خلية؛ 6 متر؛ 7-وحدة التحكم والبرمجة؛ 8-العرض.
تم إثبات إمكانية تخليق المرحلة الصلبة من خلال تخليق الريبونوكلياز A (R. Merrifield، 1969) وهرمون النمو البشري (D. Yamashiro، 1970)، بطول 124 و183 من الأحماض الأمينية، على التوالي. ومع ذلك، نظرًا للسباق الصغير ولكن المستمر الذي يحدث أثناء تكوين الرابطة الببتيدية، فإن المركب. البروتينات لديها بيول منخفض. النشاط، وبالتالي تلقائي. يتم استخدام المُركِّبات بواسطة Ch. وصول. للحصول على عديدات ببتيدات قصيرة (10-30 وصلة)، بما في ذلك التحضيرية
يتعلق الاختراع بطريقة طور صلب لتخليق ببتيد بالصيغة H-D--Nal--Thr-NH 2، والذي يستخدم كلاً من الأحماض الأمينية المحمية بـ Boc والمحمية بـ Fmoc وراتنج بوليسترين مكلور ميثيل. 10 ز.ب. يطير.
مجال التكنولوجيا الذي ينتمي إليه الاختراع
يتعلق الاختراع الحالي بطريقة لتحضير ببتيد يحتوي على ثلاثة أو أكثر من بقايا حمض أميني، مع حمض أميني طرفي N، وحمض أميني قبل الأخير مجاور للحمض الأميني طرفي N، وحمض أميني طرفي C.
فن مسبق
تم تقديم تخليق الببتيد في الطور الصلب في عام 1963 للتغلب على العديد من مشكلات خطوات التنقية الوسيطة المرتبطة بتخليق محلول الببتيدات (ستيوارت وآخرون. تخليق الببتيد في الطور الصلب. شركة بيرس الكيميائية، الطبعة الثانية، 1984). في تخليق الطور الصلب، يتم تجميع الأحماض الأمينية (على سبيل المثال، الانضمام) إلى الببتيد في أي تسلسل مرغوب، بينما يتم ربط أحد طرفي السلسلة (على سبيل المثال، الطرف C) بحامل غير قابل للذوبان. بمجرد تجميع التسلسل المطلوب على الحامل (الدعم)، يتم بعد ذلك تحرير الببتيد (أي انشقاقه) من الحامل. مجموعتا الحماية القياسيتان لمجموعات α-amino من الأحماض الأمينية المراد ربطها هما Boc، الذي تتم إزالته بحمض قوي، وFmoc، الذي تتم إزالته بقاعدة. يتعلق الاختراع الحالي بطريقة ملائمة لإنتاج الببتيدات باستخدام مزيج من كل من وسائل الحماية هذه لمجموعات α-amino في تخليق واحد على راتنج غير مكلف من بوليسترين مكلور الميثيل.
عند تصميم تخليق الببتيد في الطور الصلب باستخدام أي من أنظمة الحماية الأمينية ألفا المذكورة أعلاه، من المهم أن يتم حماية أي "مجموعات جانبية" تفاعلية من الأحماض الأمينية التي تشكل الببتيد من التفاعلات الكيميائية غير المرغوب فيها أثناء تجميع السلسلة. ومن المرغوب أيضًا ألا تتم إزالة المجموعات الكيميائية المختارة لحماية المجموعات الجانبية المختلفة بواسطة الكواشف المستخدمة لإزالة حماية مجموعات .beta.-amino. ثالثًا، من المهم أن تكون رابطة سلسلة الببتيد المتنامية بجسيمات الراتينج مقاومة للكواشف المستخدمة في عملية تجميع السلسلة لإزالة أي نوع من الحماية الأمينية ألفا. في حالة نظام حماية α-amino باستخدام Fmoc، يجب أن تكون حماية المجموعة الجانبية مقاومة للكواشف القلوية المستخدمة لإزالة Fmoc. من الناحية العملية، عادةً ما تتم إزالة مجموعات حماية السلسلة الجانبية هذه باستخدام كواشف حمضية خفيفة بعد اكتمال تجميع سلسلة الببتيد. إذا تم استخدام نظام حماية مجموعة β-amino باستخدام Boc، فيجب أن تكون حماية المجموعة الجانبية مقاومة للكاشف الحمضي الضعيف المستخدم لإزالة مجموعة Boc في كل دورة. في الممارسة العملية، عادةً ما تتم إزالة مجموعات حماية السلسلة الجانبية هذه في نظام الحماية الأمينية بيتا مع Boc باستخدام HF اللامائي بعد اكتمال تجميع سلسلة الببتيد. وبالتالي، من الناحية العملية، فإن مجموعات حماية السلسلة الجانبية شائعة الاستخدام في نظام حماية α-amino مع Fmoc ليست مستقرة في ظل الظروف المستخدمة لإزالة حماية مجموعات α-amino مع Boc. ولذلك، لا يتم الجمع بين نوعين من مخططات الحماية لمجموعات ألفا أمينو أثناء تجميع سلسلة الببتيد في تخليق الببتيد في المرحلة الصلبة. بالإضافة إلى ذلك، على الرغم من أن أرخص راتينج بوليمر يستخدم في تخليق الببتيد (البوليسترين المكلور أو "راتنج ماريفيلد") يستخدم على نطاق واسع مع الأحماض الأمينية المحمية بواسطة مجموعات Boc، فقد تم التوصل في الأدبيات إلى أنه لا ينطبق في حالة الحماية مجموعات ألفا أمينو مع مجموعات Fmoc بسبب عدم استقرارها في ظل الظروف القلوية (انظر ستيوارت وآخرون. تركيب الببتيد في المرحلة الصلبة. شركة بيرس الكيميائية، الطبعة الثانية، 1984). يتم توجيه الاختراع الحالي إلى طريقة للاستخدام المشترك لبعض الببتيدات في تخليق الطور الصلب لكل من الأحماض الأمينية المحمية بـ Boc والأحماض الأمينية المحمية بـ Fmoc على راتينج Merifield.
من المعروف أن Lanreotide®، وهو نظير السوماتوستاتين، يمنع إطلاق هرمون النمو ويمنع أيضًا إفراز الأنسولين والجلوكاجون وإفراز البنكرياس الخارجي.
براءة الاختراع الأمريكية رقم 4,853,371 تكشف وتطالب بـ Lanreotide®، وهي عملية لتحضيره، وطريقة لتثبيط إفراز هرمون النمو، والأنسولين، والجلوكاجون، وإفراز البنكرياس الخارجي.
تكشف براءة الاختراع الأمريكية رقم 5147856 عن استخدام Lanreotide® لعلاج عودة التضيق.
براءة الاختراع الأمريكية رقم 5411943 تكشف عن استخدام Lanreotide® لعلاج سرطان الكبد.
براءة الاختراع الأمريكية رقم 5073541 تكشف عن استخدام Lanreotide® لعلاج سرطان الرئة.
يكشف طلب براءة الاختراع الأمريكية رقم 08/089410، الذي تم تقديمه في 9 يوليو 1993، عن استخدام Lanreotide® لعلاج سرطان الجلد.
تكشف براءة الاختراع الأمريكية رقم 5,504,069 عن استخدام Lanreotide® لمنع نمو الورم الصلب المتسارع.
يكشف طلب براءة الاختراع الأمريكية رقم 08/854941، الذي تم تقديمه في 13 مايو 1997، عن استخدام Lanreotide® لإنقاص الوزن.
يكشف طلب براءة الاختراع الأمريكية رقم 08/854,943، الذي تم تقديمه في 13 مايو 1997، عن استخدام Lanreotide® لعلاج مقاومة الأنسولين والمتلازمة X.
تكشف براءة الاختراع الأمريكية رقم 5688418 عن استخدام Lanreotide® لإطالة عمر خلايا البنكرياس.
يكشف طلب معاهدة التعاون بشأن البراءات رقم PCT/US 97/14154 عن استخدام Lanreotide® لعلاج التليف.
يكشف طلب براءة الاختراع الأمريكية رقم 08/855311، الذي تم تقديمه في 13 مايو 1997، عن استخدام Lanreotide® لعلاج فرط شحميات الدم.
يكشف طلب براءة الاختراع الأمريكية رقم 08/440061، الذي تم تقديمه في 12 مايو 1995، عن استخدام Lanreotide® لعلاج فرط اميلين الدم.
يكشف طلب براءة الاختراع الأمريكية رقم 08/852221، الذي تم تقديمه في 7 مايو 1997، عن استخدام Lanreotide® لعلاج فرط برولاكتين الدم والأورام البرولاكتينية.
جوهر الاختراع
يوفر الاختراع الحالي طريقة لتحضير ببتيد يحتوي على ثلاثة أو أكثر من بقايا حمض أميني، يحتوي على حمض أميني طرفي N، وحمض أميني قبل الأخير مجاور للحمض الأميني طرفي N، وحمض أميني طرفي C، تشتمل الطريقة المذكورة على الخطوات التالية:
(أ) ربط الحمض الأميني الأول بالراتنج الداعم الصلب بواسطة رابطة أثير لتكوين منتج الاقتران الأول، والذي يتضمن (1) تفاعل محلول مائي من كربونات السيزيوم مع محلول كحولي للحمض الأميني الأول لتكوين ملح السيزيوم. من الحمض الأميني الأول، (2) الحصول على ملح السيزيوم الخالي من المذيبات من الحمض الأميني الأول، (3) تفاعل راتنج الدعم الصلب مع ملح السيزيوم من الحمض الأميني الأول في مذيب قطبي جاف (لا مائي) لتكوين منتج الإضافة الأول،
حيث يتوافق الحمض الأميني الأول مع الحمض الأميني الطرفي C للببتيد، ويتم حظر المجموعة الأمينية من السلسلة غير الجانبية (الرئيسية) للحمض الأميني الأول بواسطة Boc، ولا يحتوي الحمض الأميني الأول على مجموعة وظيفية في السلسلة الجانبية التي تتطلب الحماية، والدعم الصلب - الراتنج - عبارة عن راتنج من البوليسترين المكلور؛
(ب) إزالة الحماية (إزالة الحظر) Boc من منتج المدخل الأول مع حمض لتكوين منتج مزيل الحظر من المدخل الأول؛
(ج) اختياريًا، ربط الحمض الأميني التالي بمنتج المرفق الأول الذي تم إزالة الحظر عنه، والذي يتضمن تفاعل الحمض الأميني التالي مع منتج المرفق الأول الذي تم إزالة الحظر عنه في مذيب عضوي يحتوي على كاشف نمو الببتيد للحصول على منتج المرفق التالي المحظور (المحمي)، حيث يحتوي الحمض الأميني التالي في السلسلة الرئيسية على مجموعة أمينية محجوبة بواسطة Boc، وإذا كان الحمض الأميني التالي يحتوي على مجموعة وظيفية واحدة أو أكثر في السلسلة الجانبية، فإن المجموعات الوظيفية في السلسلة الجانبية لا تحتاج إلى حماية أو المجموعات الوظيفية تحتوي السلسلة الجانبية على مجموعات واقية مقاومة للكواشف الحمضية أو القلوية المستخدمة لإزالة الحماية، على التوالي، Boc وFmoc؛
(د) إزالة حماية Boc من المقاربة التالية المحجوبة، والتي تتضمن تفاعل المقاربة التالية المحجوبة مع حمض للحصول على المقاربة التالية غير المحمية؛
(هـ) اختياريًا، تكرار الخطوتين (ج) و(د)، حيث تولد كل دورة منتجًا تم إصداره للمرفق التالي (X+1)، حيث X هو رقم التكرار المطلوب للدورة؛
(و) إضافة الحمض الأميني التالي إلى منتج الملحق الأول المحرر من الخطوة (ب) أو، اختياريًا، إلى منتج الملحق التالي (X+1) المحرر من الخطوة (هـ)، والذي يتضمن تفاعل الحمض الأميني التالي مع المذكور منتج المرفق الأول أو مع المنتج المحدد الذي تم إزالة الحظر عنه من (X+1) - المدخل التالي في مذيب عضوي يحتوي على كاشف لتنمية الببتيد للحصول على منتج محجوب (محمي) من المدخل التالي، ويكون للحمض الأميني التالي مجموعة أمينية Fmoc محجوبة من السلسلة الرئيسية، بشرط أنه إذا كان الحمض الأميني التالي يحتوي على مجموعة وظيفية واحدة أو أكثر في السلسلة الجانبية، فإن المجموعات الوظيفية في السلسلة الجانبية لا تحتاج إلى حماية، أو المجموعات الوظيفية في السلسلة الجانبية لديها مجموعات الحماية المقاومة للكواشف القلوية المستخدمة لإزالة حماية Fmoc؛
(ز) إزالة حماية Fmoc من المقاربة التالية المحجوبة، والتي تتضمن تفاعل المقاربة التالية المحجوبة مع أمين أولي أو ثانوي للحصول على المقاربة التالية غير المحمية؛
(ح) اختياريًا، تكرار الخطوتين (هـ) و(ز)، حيث تولد كل دورة منتجًا محظورًا للإضافة التالية (X+1)، حيث X هو رقم التكرار الضروري للدورة، حتى الدورة قبل الأخيرة يتم تضمينه في الببتيد والأحماض الأمينية المحظورة.
(i) ربط الحمض الأميني الطرفي N بمنتج المدخل التالي المنزوع الحماية (X+1)، والذي يتضمن تفاعل الحمض الأميني الطرفي N مع منتج المدخل التالي المنزوع الحماية (X+1) في مذيب عضوي يحتوي على كاشف نمو الببتيد، للحصول على منتج نهائي محجوب، حيث يحتوي الحمض الأميني N-terminal على مجموعة أمينية أساسية محجوبة بواسطة Boc أو Fmoc؛
(ي) إزالة حماية Boc أو Fmoc من منتج الإضافة المكتملة المحظورة، بما في ذلك تفاعل منتج الإضافة المكتملة المحظورة مع حمض في حالة Boc أو قاعدة في حالة Fmoc لتكوين منتج الببتيد المكتمل على الراتينج؛
(ي) إذا كان منتج الببتيد المكتمل على الراتينج يحتوي على مجموعات وظيفية ذات سلسلة جانبية، عندئذٍ يتم اختياريًا إزالة حماية المجموعات الوظيفية للسلسلة الجانبية لمنتج الببتيد المكتمل على الراتينج، والذي يتضمن تفاعل منتج الببتيد المكتمل على الراتينج باستخدام كواشف إزالة الحماية المناسبة للحصول على منتج الببتيد المكتمل على الراتنج تمت إزالة الحماية; و
(ك) فصل الببتيد من حامل الراتينج الصلب لمنتج الببتيد المكتمل على الراتينج أو منتج الببتيد المكتمل على الراتينج منزوع الحماية للحصول على الببتيد، والذي يشتمل على تفاعل منتج الببتيد المكتمل على الراتينج أو منتج الببتيد المكتمل على الراتينج منزوع الحماية مع الأمونيا ، أمين أولي أو أمين ثانوي للإكمال العملي لانقسام الببتيد من الراتنج؛
بشرط أن يتم تنفيذ الخطوتين (هـ) و (ز) في تركيب الببتيد مرة واحدة على الأقل.
المفضلة هي العملية وفقًا للاختراع الحالي حيث تكون الأمونيا، الأمين الأولي أو الأمين الثانوي في الخطوة (ك) في مذيب يحتوي على كحول ومذيب قطبي لابروتيك اختياريًا،
تُفضل الطريقة وفقًا للاختراع الحالي، حيث تشتمل الخطوة (ل) أيضًا على الخطوات التالية:
ترسيب الببتيد المشقوق من المذيب؛
يتم الفصل عن طريق الترشيح بين الدعامة الراتنجية الصلبة والببتيد المترسب، و
استخلاص الببتيد بمحلول حمضي لعزل الببتيد.
تُفضل الطريقة وفقًا للاختراع الحالي، حيث يكون الحمض الأميني الأول هو Boc-L-Thr.
المفضلة هي الطريقة وفقًا للاختراع الحالي، حيث يكون الحمض الأميني الأول هو ملح السيزيوم لـ Boc-L-Thr، مما ينتج عنه راتنج Boc-L-Thr كمنتج اقتران أول، ومنتج الاقتران الأول المزيل الكتلي هو راتينج H-L-Thr .
المفضلة هي عملية الاختراع الحالي حيث يكون الحمض المستخدم لإزالة مجموعة الحماية Boc في الخطوة (الخطوات) هو حمض ثلاثي فلورو أسيتيك (TFA).
الطريقة المفضلة، المرتبطة بالعملية السابقة مباشرة، هي حيث يكون المذيب العضوي هو كلوريد الميثيلين، أو الكلوروفورم، أو ثنائي ميثيل فورماميد وكاشف نمو الببتيد هو ثنائي إيزوبروبيل كاربوديميد، أو ثنائي سيكلوهيكسيل كاربوديميد، أو N- إيثيل- ن" - (3- ثنائي ميثيل - أمينوبروبيل) كاربوديميد .
الطريقة المفضلة، المتعلقة بالطريقة السابقة مباشرة، هي طريقة تشتمل على تنفيذ الخطوتين (هـ) و(ز) ست مرات بعد تكوين منتج اقتران أول تم إزالة انسداده بالصيغة H-L-Thr-resin، حيث تكون الأحماض الأمينية اللاحقة مرفقة بالترتيب: Fmoc-L-Cys( Acm)، Fmoc-L-Val، Fmoc-L-Lys(Boc)، Fmoc-D-Trp، Fmoc-L-Tyr(O-t-Bu) وFmoc-L- Cys(Acm) لتكوين المنتج H-Cys(Acm)-Tyr(O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-الراتنج.
الطريقة المفضلة، المتعلقة بالطريقة السابقة مباشرة، هي طريقة تشتمل على إضافة Boc-D--Nal إلى H-Cys(Acm)-Tyr(O-t-Bu)-D-Trp-Lys(Boc)-Val- Cys(Acm) -Tnr-راتنج وفقًا للخطوة (ج) للحصول على Boc-D--Nal-Cys(Acm)-Tyr(O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Ast) -Thr-الراتنج.
تتضمن الطريقة المفضلة، المرتبطة بالطريقة السابقة مباشرة، الإزالة المتزامنة لمجموعة Boc التي تحمي D--Nal، ومجموعة O-t-Bu التي تحمي Tyr، ومجموعة Boc التي تحمي Lys في Boc-D--Nal-Cys(Acm) )-Tyr( O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-الراتنج وفقًا للخطوة (i)، للحصول على منتج الببتيد المكتمل على راتينج الصيغة H-D- - نال-Cys(Acm)-Tyr- D-Trp-Lys-Val-Cys(Acm)-Thr-الراتنج.
تشتمل الطريقة المفضلة، المرتبطة بالطريقة السابقة مباشرة، على انقسام الببتيد H-D-β-Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr من الراتنج الصلب عن طريق تنفيذ تفاعل H-D-βNal-Cys (Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-راتنج مع الأمونيا في مذيب يحتوي على كحول واختياريًا مذيب قطبي لابروتيك للتخلص الكامل إلى حد كبير لإعطاء H-D --Nal-Cys (Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-NH 2 .
العملية المفضلة، المتعلقة بالعملية السابقة مباشرة، هي حيث يكون الكحول ميثانول والمذيب اللابروتيكي القطبي هو ثنائي ميثيل فورماميد.
تتضمن الطريقة المفضلة، المرتبطة بالطريقة السابقة مباشرة، الإزالة المتزامنة لمجموعات Cys التي تحمي Acm ودورة بقايا Cys غير المحمية الناتجة في منتج الببتيد المكتمل بالصيغة H-D--Nal-Cys(Acm)-Tyr-D -Trp-Lys-Val -Cys(Acm)-Thr-NH 2 عن طريق تنفيذ تفاعل H-D- -Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-NH 2 بمحلول اليود في الكحول إلى إزالة الحماية والدورنة بشكل شبه كامل ليعطي H-D--Nal-Thr-NH 2 .
الطريقة المفضلة، المرتبطة بالطريقة السابقة مباشرة، هي الطريقة التي يكون فيها الببتيد H-D--Nal-Thr-NH 2 .
الطريقة المفضلة، المتعلقة بالطريقة السابقة مباشرة، هي الطريقة التي يكون فيها الببتيد نظير السوماتوستاتين.
يتم تعريف المصطلحات المستخدمة في وصف الاختراع الحالي على النحو التالي:
"الحمض الأميني الأول": يشمل أي حمض أميني تكون فيه المجموعة الأمينية في السلسلة الرئيسية (وليس في السلسلة الجانبية) محمية بواسطة Boc، وهو منتج تجاري أو يمكن تصنيعه وفق طرق معروفة لشخص ذي مهارة عادية. في الفن، على سبيل المثال Boc-L-Thr؛
"منتج المرفق الأول": يصف المنتج المرتبط براتنج حامل صلب ينتج عن إضافة حمض أميني أول إلى راتنج حامل صلب، على سبيل المثال راتينج Boc-L-Thr؛
"منتج الاقتران الأول الذي تم إزالة حظره": يصف المنتج الناتج عن إزالة أو إزالة مجموعة Boc من منتج الاقتران الأول - على سبيل المثال، H-L-Thr-resin، حيث "H" هو الهيدروجين المتوفر للمجموعة الأمينية الرئيسية السلسلة الناتجة عن خطوة إزالة الحماية؛
"الحمض الأميني التالي": يصف أي حمض أميني تكون فيه المجموعة الأمينية في السلسلة الرئيسية محمية بواسطة Boc أو Fmoc، والذي يكون متاحًا تجاريًا أو يمكن تصنيعه وفقًا للطرق المعروفة لأحد ذوي المهارات العادية في المجال. نظرًا لأنه يمكن تضمين الخطوة (ج) والخطوة (هـ) في دورة متكررة حيث يتم تنفيذ الخطوة أكثر من مرة، في كل مرة يتم تنفيذ الخطوة (ج) أو الخطوة (هـ)، يمكن اختيار "الحمض الأميني التالي" بشكل مستقل من مجموعة معروفة أو من المحتمل أن تكون أحماض أمينية مركبة تكون فيها المجموعة الأمينية في السلسلة الرئيسية محمية بواسطة Boc أو Fmoc؛
"المنتج المحظور للمدخل التالي (X + 1)": يصف المنتج المرتبط بالراتنج الداعم الصلب، وهو نتيجة اتصال الحمض الأميني التالي مع "المنتج المحظور للمدخل التالي". بما أنه يمكن تضمين الخطوتين (ج) و(د) والخطوتين (هـ) و(ز) في دورة متكررة حيث يمكن ربط الأحماض الأمينية التالية، فإن المصطلح "المنتج المحظور للملحق التالي (X+1)" يشير إلى المنتج الذي تم الحصول عليه نتيجة لكل دورة من دورات الانضمام السابقة؛
"المنتج غير المحظور للمدخل التالي (X+1)": يصف المنتج الناتج عن إزالة مجموعة Fmoc من "المنتج المحظور للمدخل التالي (X+1)"؛
"منتج الببتيد المكتمل على الراتينج": يصف منتج الببتيد المرتبط براتنج دعم صلب بعد ربط حمض أميني طرفي N بسلسلة الببتيد وبعد إزالة حماية المجموعة الأمينية للعمود الفقري للحمض الأميني N-terminal أو رفع حظرها ، ولكن لا يزال لديه أي مجموعات حماية على المجموعات الوظيفية للسلاسل الجانبية، لم تتم إزالتها بواسطة التفاعل، مما يؤدي إلى إزالة المجموعة الواقية من السلسلة الرئيسية للحمض الأميني N-terminal؛ و
"منتج ببتيد مكتمل على راتينج منزوع الحماية": يصف منتج ببتيد متصل بدعامة راتنجية صلبة حيث تمت إزالة جميع مجموعات الحماية أو إزالة حمايتها من المجموعات الوظيفية للسلاسل الجانبية للأحماض الأمينية.
من أمثلة الأحماض التي يمكن استخدامها لإزالة حماية Boc حمض ثلاثي فلورو أسيتيك (TFA)، وحمض الميثان سلفونيك، والمحاليل العضوية التي تحتوي على حمض الهيدروكلوريك.
من أمثلة الأمينات الأولية والثانوية التي يمكن استخدامها لإزالة حماية Fmoc هي 4-(أمينوميثيل)بيبريدين، بيبيريدين، ثنائي إيثيل أمين، DBU وتريس(2-أمينو إيثيل) أمين.
أمثلة على القواعد غير المحبة للنواة التي يمكن استخدامها لتحييد أملاح TFA للمجموعات الأمينية المحررة (RNH 3 + CF 3 COO - يجب تحويل هذه الأملاح إلى أمينات "حرة" (NH 2) قبل أو أثناء إضافة الحمض الأميني التالي ، وإلا فلن تتم الإضافة) هما ثنائي إيزوبروبيل إيثيل أمين (DIEA) وثلاثي إيثيل أمين (TEA).
أمثلة على المذيبات العضوية التي يمكن استخدامها في تفاعلات إضافة الأحماض الأمينية هي كلوريد الميثيلين، الكلوروفورم، ثنائي كلورو الإيثان، ثنائي ميثيل فورماميد، ثنائي إيثيل أسيتاميد، رباعي هيدروفيوران، أسيتات الإيثيل، 1-ميثيل-2-بيروليدون، أسيتونيتريل، أو مزيج من هذه المذيبات.
تشتمل أمثلة موسعات الببتيد على كربوديمايدات مستبدلة مثل: ثنائي إيزوبروبيل كاربوديميد، ثنائي سيكلوهكسيل كاربوديميد، أو N-إيثيل-ن'-(3-ديميثيل أمينوبروبيل) كاربوديميد.
يُشار إلى مجموعات الكربوكسيل والمجموعات الأمينية التي تشارك في تكوين رابطة أميد الببتيد باسم مجموعة الكربوكسيل "السلسلة الجانبية" أو المجموعة الأمينية، على التوالي. من ناحية أخرى، أي مجموعات وظيفية من الأحماض الأمينية لا تشارك في تكوين رابطة أميد الببتيد يشار إليها باسم المجموعات الوظيفية "السلسلة الجانبية".
يشير مصطلح "المجموعة المقاومة للقاعدة" إلى المجموعات المحمية المستخدمة لحماية المجموعات الوظيفية للأحماض الأمينية التي (1) مقاومة للقاعدة، على سبيل المثال، لا يمكن إزالتها بواسطة قواعد مثل 4-(أمينو إيثيل) بيبيريدين، أو بيبيريدين، أو تريس (2). -أمينو إيثيل) أمين، وهي قواعد شائعة الاستخدام لإزالة مجموعة الحماية Fmoc، و(2) يمكن إزالتها بحمض مثل حمض ثلاثي فلورو أسيتيك أو بطريقة أخرى مثل الهدرجة الحفزية.
يتم استخدام الرمزين "Fmoc" و"Boc" هنا وفي الصيغة المصاحبة للإشارة إلى 9-فلورينيل ميثوكسي كربونيل وt-بوتيلوكسي كربونيل، على التوالي.
يمكن استخدام الطريقة الموصوفة أعلاه لتحضير الببتيدات، ويفضل نظائر السوماتوستاتين، مثل Lanreotide® octapeptide، الذي له الصيغة التالية: H-D--Nal--Thr-NH 2. إذا كان سيتم تصنيع H-D--Nal--Thr-NH 2، فإن مجموعات الحماية المقاومة للقاعدة المستخدمة لحماية المجموعات الوظيفية للسلسلة الجانبية Cys وLys وTyr يمكن أن تكون أسيتاميدوميثيل (Acm) وBoc وtert-butyl، على التوالي. يفضل Asm على Cys.
يُقصد بنظير السوماتوستاتين الببتيد الذي يُظهر نشاطًا بيولوجيًا مشابهًا (أي ناهض) أو معاكسًا (أي مضادًا) لنشاط السوماتوستاتين.
في الصيغة H-D--Nal--Thr-NH 2، يشير كل رمز من رموز الأحماض الأمينية المعتادة المكونة من ثلاثة أحرف (على سبيل المثال، Lys) إلى بقايا حمض أميني هيكلي. على سبيل المثال، يمثل الرمز Lys في الصيغة أعلاه -NH-CH((CH 2) 4 NH 2)-CO-. يمثل الرمز D- -Nal- بقايا الأحماض الأمينية D-2-naphthylalanilyl. تشير الأقواس إلى رابطة ثاني كبريتيد تربط الثيول الحر لاثنين من بقايا Cys في الببتيد، مما يشير إلى أن الأحماض الأمينية للببتيد داخل الأقواس تشكل دورة.
بناءً على الوصف الوارد هنا، سيكون الشخص الماهر في المجال قادرًا على استخدام الاختراع الحالي بشكل كامل.
ما لم يتم تحديد خلاف ذلك، فإن جميع المصطلحات التقنية والعلمية المستخدمة هنا لها نفس المعنى الذي يفهمه عادةً أصحاب المهارة العادية في المجال الذي يتعلق به الاختراع الحالي. بالإضافة إلى ذلك، تم دمج جميع المنشورات وطلبات براءات الاختراع وبراءات الاختراع والمراجع الأخرى المذكورة هنا بالإشارة إليها.
يمكن تحضير الببتيد وفقًا لطريقة الاختراع الحالي وفقًا للإجراء التالي.
تتم إضافة محلول من 0.5 مولاري من كربونات السيزيوم في الماء ببطء إلى محلول من 1 مكافئ مولي من Boc-AA 1 (باكيم كاليفورنيا، تورانس، كاليفورنيا) حيث يقابل AA 1 الحمض الأميني الطرفي C المذاب في الكحول، ويفضل الميثانول. تم تقليب الخليط الناتج لمدة ساعة واحدة تقريبًا عند درجة حرارة الغرفة، ثم تمت إزالة كل الكحول وكل الماء تحت ضغط مخفض لإعطاء مسحوق جاف من ملح السيزيوم Boc-AA 1. يتم غسل راتينج ميريفيلد، ما يعادله 1.0 (بوليسترين ميثيل الكلور، 200-400 شبكة، دمج أيون الكلوريد 1.3 ميكروغرام/جم، Advanced ChemTech، Louisville، Kentucky أو Polymer Laboratories، Church Stretton، إنجلترا) بمذيب مكلور، ويفضل ثنائي كلورو ميثان (DCM). )، كحول، ويفضل ميثانول، ومذيب لابروتيك قطبي، ويفضل ثنائي ميثيل فورماميد (DMF). يتم إذابة مسحوق ملح السيزيوم Boc-AA 1 في مذيب لا مائي قطبي لا مائي (جاف)، ويفضل DMF، ويتم دمج المحلول مع الراتنج المغسول مسبقًا. يتم تقليب الملاط بلطف عند حوالي 45 درجة - 65 درجة مئوية، ويفضل عند 50 درجة - 60 درجة مئوية، لمدة حوالي 48 إلى 106 ساعة، ويفضل 85 إلى 90 ساعة، تحت جو خامل مثل النيتروجين. يتم فصل الراتينج بالترشيح وغسله جيدًا باستخدام مذيب لابروتيك قطبي، ويفضل DMF، وماء، وأخيرًا كحول مثل MeOH. يتم تجفيف راتينج Boc-AA 1 تحت ضغط منخفض.
يتم إدخال راتنج Boc-AA 1 في مفاعل زجاجي بقاعدة مرشح مصنوعة من الزجاج المنصهر الخشن. يتم غسل الراتينج بمذيب مكلور مثل DCM، ويتم إزالة عائقه بحمض عضوي، ويفضل 25% TFA في DCM، ويتم غسله لفترة وجيزة بمحلول مكلور مثل DCM وكحول مثل MeOH، ويتم تحييده بقاعدة عضوية، ويفضل ثلاثي إيثيل أمين في DCM، ويتم غسله مرة أخرى باستخدام DCM ومذيب لابروتيكي قطبي مثل DMF لإعطاء راتنج AA 1 منزوع الحماية.
يتم بعد ذلك ربط أي عدد مرغوب من الأحماض الأمينية بشكل اختياري براتنج AA 1 المحمي. إذا كان الحمض الأميني التالي يحتوي على مجموعة α-amino مع حماية Fmoc (Fmoc-AA x)، فإن مجموعة السلسلة الجانبية إما لا تحتاج إلى حماية (على سبيل المثال، Fmoc-Gly، Fmoc-Ala، Fmoc-Phe، أو Fmoc-). Thr) أو السلسلة الجانبية محمية بمجموعة مقاومة للقاعدة. يتم ربط فائض مولي من Fmoc-AA x (حيث x هو رقم موضع الحمض الأميني في الببتيد، المحسوب من الطرف C) لمدة 60 دقيقة تقريبًا براتنج AA 1 غير المحمي مع كاشف نمو الببتيد مثل ثنائي إيزوبروبيل كاربوديميد. (مدينة دبي للإنترنت)، في خليط DCM/DMF. تم غسل راتنج الإضافة باستخدام DMF، والكحول، وDCM لإعطاء راتنج Fmoc-AA x -AA 1. يمكن التحقق من المرفقات باستخدام طريقة كايزر نينهيدرين. بعد ذلك، يتم غسل راتينج Fmoc-AA x -AA 1 مرة واحدة باستخدام DMF ثم يتم إزالة كتلته بمحلول قاعدة في مذيب عضوي مثل البيبيريدين في DMF للحصول على راتنج AA x -AA 1. يتم بعد ذلك غسل راتينج AA x -AA 1 باستخدام DMF، يليه الغسيل عدة مرات باستخدام كل من الكحول مثل MeOH وDCM. بعد ذلك، يتم غسل راتنج AA x -AA 1 مرة واحدة باستخدام DMF لمدة 3 دقائق تقريبًا، وثلاث مرات باستخدام الأيزوبروبانول، ويفضل لمدة دقيقتين تقريبًا في كل مرة، وثلاث مرات باستخدام DCM، ويفضل لمدة دقيقتين تقريبًا في كل مرة. يصبح الراتينج جاهزًا بعد ذلك لربط إضافي إما بحمض أميني محمي بـ Fmoc كما هو موضح أعلاه أو حمض أميني محمي بـ Boc كما هو موضح أدناه.
وبالمثل، إذا تم تحديد أي حمض أميني لاحق ليتم ربطه براتنج AA 1 المزيل الحماية مع مجموعة Boc-amino المحمية (Boc-AA x)، فإما أنه لا توجد حماية مطلوبة لمجموعة السلسلة الجانبية (يمكن أن تكون Boc-Gly , Boc-Ala, Boc-Phe أو Boc-Thr) أو السلسلة الجانبية يجب أن تكون محمية بمجموعة مقاومة للإزالة بواسطة كل من الحمض والقاعدة، والتي قد تكون Boc-Cys(Acm). إذا تم تحديد Boc-AA x، فسيتم إرفاقه باستخدام نفس الكواشف والمذيبات كما هو موضح أعلاه بالنسبة للأحماض الأمينية Fmoc، ويمكن التحقق من اكتمال (اكتمال) الارتباط بواسطة طريقة Kaiser ninhydrin. بعد ذلك، تتم إزالة حماية راتنج Boc-AA x -AA 1 بمحلول حمض في مذيب عضوي مثل TFA في DCM لإعطاء راتنج CF 3 CO - H + -AA x -AA 1. يتم بعد ذلك غسل هذا الراتينج عدة مرات باستخدام مذيب مكلور مثل DCM، وكحول مثل MeOH، وتحييده باستخدام قاعدة غير محبة للنواة مثل ثلاثي إيثيل أمين في DCM، ثم يتم غسله عدة مرات أخرى باستخدام مذيب مكلور مثل DCM لإعطاء AA x -AA 1 - راتينج. يصبح الراتينج جاهزًا بعد ذلك لربط المزيد من الأحماض الأمينية Boc أو Fmoc المحمية كما هو موضح أعلاه.
اعتمادًا على التسلسل المطلوب من الببتيد ونوع الحمض الأميني المحمي α-amino المستخدم (إما المحمي Fmoc أو المحمي Boc)، يتم استخدام مجموعة مناسبة من إجراءات الارتباط المذكورة أعلاه، اعتمادًا على الحمض الأميني الذي سيتم تنفيذه في تسلسل الببتيد - سلسلة جانبية، تحتوي على مجموعة وقائية يمكن إزالتها إما بالقاعدة اللازمة لإزالة Fmoc من مجموعة α-amino، أو الحمض الضروري لإزالة Boc من مجموعة α-amino. مثل هذا الحمض الأميني المحمي قد يكون N-β-Boc-N″-β-Fmoc-lysine أو N-β-Fmoc-N″-β-Boc-lysine. إذا كان الأمر كذلك، فإن جميع مجموعات الحماية القابلة للتحديد للمجموعات الأمينية α للأحماض الأمينية اللاحقة، حتى الحمض الأميني الطرفي N، يجب أن تكون متوافقة مع حماية المجموعة الجانبية المحددة لهذا الموضع. وهذا يعني أن مجموعات حماية السلسلة الجانبية يجب أن تكون مقاومة لعامل إزالة الحظر المستخدم لإزالة حماية مجموعات α-amino من الأحماض الأمينية اللاحقة. بالنسبة للحمض الأميني N-terminal، يمكن استخدام إما Boc أو Fmoc كحماية أمينية α، نظرًا لأن إزالة حماية الحمض الأميني N-terminal يمكن أن يؤدي في الوقت نفسه إلى إزالة حماية بعض السلاسل الجانبية المحمية دون التأثير بشكل غير مرغوب فيه على استراتيجية تخليق الببتيد، حيث لا الأحماض الأمينية متوفرة بعد الآن.
يجب إزالة الحماية وإطلاق سلسلة الببتيد المكتملة، والتي لا تزال متصلة بالراتنج. لإزالة جميع مجموعات الحماية المقاومة للقاعدة ومجموعة الحجب الأمينية α للحمض الأميني الطرفي N، إن أمكن، تتم معالجة الببتيد الموجود على الراتينج بحمض في مذيب عضوي مثل TFA في DCM. لإزالة أي مجموعات حماية مقاومة للأحماض ومجموعة الحجب الأمينية α للحمض الأميني N-terminal، إن أمكن، تتم معالجة الببتيد الموجود على الراتينج بقاعدة عضوية مثل البيبيريدين في DMF. وبدلاً من ذلك، يمكن الاحتفاظ بالمجموعات المقاومة للحمض حتى تتم إزالتها عند الانقسام اللاحق للببتيد باستخدام الأمونيا أو قاعدة أمين. يتم بعد ذلك غسل الببتيد الموجود على الراتينج المنزوع الحماية باستخدام مذيب مكلور مثل DCM، وكحول مثل MeOH وتجفيفه إلى وزن ثابت تحت ضغط منخفض.
يتم شق الببتيد من الراتينج ويتم تحويل الطرف C إلى الأميد عن طريق تعليق الببتيد على الراتنج في 3:1 MeOH/DMF. يتم تبريد الملاط إلى درجة حرارة أقل من حوالي 10 درجات مئوية. تحت جو من النيتروجين ويتم إدخال غاز الأمونيا اللامائي تحت سطح المذيب حتى يتشبع المحلول به، مع الحفاظ على درجة الحرارة أقل من حوالي 10 درجات مئوية. يتم تقليب الملاط بلطف لمدة 24 ساعة تقريبًا مع السماح لدرجة الحرارة بالارتفاع إلى حوالي 20 درجة مئوية. يتم التحقق من درجة اكتمال التفاعل من خلال اختفاء إستر الميثيل الوسيط في HPLC تحت ظروف مناسبة حسب نوع الببتيد. تفاعل مزيجيقم بتبريده وإضافة الكمية المطلوبة من الأمونيا اللامائية حتى تصبح منطقة ذروة HPLC المقابلة لإستر الميثيل أقل من 10% من مساحة الذروة للمنتج المستهدف. يتم تبريد الملاط إلى أقل من حوالي 10 درجات مئوية ويستمر التحريك طوال الليل لترسيب الببتيد. يتم فصل الراسب والراتنج عن طريق الترشيح وغسلهما باستخدام MeOH البارد. يتم تجفيف الراسب والراتنج تحت ضغط مخفض، ويتم استخلاص المنتج من الراتينج بمحلول مائي من حمض الأسيتيك.
إذا كان الببتيد يحتوي على بقايا Cys محمية في تسلسله، يمكن إزالة حماية مجموعات الثيول وتدوير البقايا وفقًا للإجراء التالي. يذوب الببتيد المحتوي على مجموعات Asm المحمية من Cys في محلول مائي من حمض الأسيتيك تحت جو من النيتروجين. يقلب المحلول بسرعة ويضاف محلول اليود في الكحول في حصة واحدة. يتم تقليب الخليط وفحصه بواسطة HPLC لإزالة الحماية الكاملة. ثم يتم إيقاف التفاعل بالمعايرة بمحلول ثيوكبريتات الصوديوم 2% حتى يختفي لون المحلول. تمت تنقية الخليط الخام بواسطة تحليل كروماتوجرافي تحضيري على خرطوشة C8 مع تدرج من الأسيتونيتريل في محلول أسيتات أمونيوم 0.1، وتم تحليته على خرطوشة C8 مع تدرج من الأسيتونيتريل في 0.25 N حمض أسيتيك، وتم تجفيفه بالتجميد لإعطاء الببتيد المستهدف.
تجسيد مثالي للاختراع
يتم توفير المثال التالي لتوضيح طريقة الاختراع الحالي ولا ينبغي تفسيره على أنه يحد من نطاقه.
مثال 1. H 2 -D- -Nal--Thr-NH 2
أ) بوك-L-Thr-الراتنج
تمت إضافة ببطء محلول 2.58 جم من كربونات السيزيوم في 2.5 مل من الماء إلى محلول 3.48 جم من Boc-L-ثريونين (Bachem California، Torrance، CA) المذاب في 7 مل من الميثانول. تم تقليب الخليط الناتج لمدة ساعة واحدة تقريبًا عند درجة حرارة الغرفة، ثم تمت إزالة كل الميثانول وكل الماء تحت ضغط مخفض لإعطاء مسحوق جاف من ملح السيزيوم Boc-L-threonine. تم غسل 10 جم من راتينج ماريفيلد (بوليسترين مكلور الميثيل، شبكة 200-400، دمج الكلور 1.3 ميكروغرام/جم، Advanced ChemTech، Louisville، Kentucky) باستخدام ثنائي كلورو ميثان (DCM)، وميثانول (MeOH) وثنائي ميثيل فورماميد (DMF) (كل مرتين 70 مل). تم إذابة مسحوق ملح السيزيوم Boc-L-threonine في 60 مل من DMF الجاف وتم دمج المحلول مع الراتينج المغسول على النحو الوارد أعلاه. تم تقليب الملاط بلطف عند درجة حرارة حوالي 50 درجة - 60 درجة مئوية لمدة 85 إلى 90 ساعة تقريبًا تحت جو من النيتروجين. تم فصل الراتينج عن طريق الترشيح وغسله جيدًا باستخدام DMF والماء منزوع الأيونات وأخيراً باستخدام MeOH. تم تجفيف راتينج Boc-threonine تحت ضغط مخفض عند حوالي 40 درجة مئوية. كان إدراج الثريونين 0.85 ± 0.15 مكافئ / جرام من الراتنج الجاف.
ب) H-D- -Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-الراتنج
تم إدخال 2.0 جم من راتنج Boc-threonine من الخطوة (A) في مفاعل زجاجي سعة 50 مل مع قاع مرشح زجاجي خشن منصهر (تحميل 1.74 مليمول). تم غسل الراتينج مرتين باستخدام DCM (20 مل)، في كل مرة لمدة 5 دقائق تقريبًا، وتم إزالة كتلته باستخدام 25% TFA في DCM (30 مل) - المرة الأولى لمدة دقيقتين تقريبًا والمرة الثانية لمدة 25 دقيقة تقريبًا، وتم غسله 3 مرات لمدة دقيقتين تقريبًا DCM (20 مل)، أيزوبروبانول (20 مل) وDCM (20 مل)، تمت معادلة مرتين لمدة 5 دقائق تقريبًا مع 10% ثلاثي إيثيل أمين في DCM (20 مل)، تم غسلها 3 مرات لمدة دقيقتين تقريبًا باستخدام DCM وغسله مرة واحدة باستخدام DMF (20 مل) لمدة 5 دقائق تقريبًا.
تمت إضافة 1.8 جم (4.35 مليمول، 2.5 مكافئ) إلى الراتينج المنزوع الكتلة من Fmoc-L-cysteine(Acm) (Bachem، CA) و683 ميكرولتر (4.35 مليمول، 2.5 مكافئ) من ثنائي إيزوبروبيل- كاربوديميد (DIC) في 14 مل من 2:1 DCM/DMF لمدة ساعة واحدة تقريبًا ودقيقتين DXM (20 مل). تم التحقق من الارتباط بواسطة طريقة كايزر نيهيدرين.
بعد التثبيت، تم غسل الراتينج مرة واحدة باستخدام DMF ومن ثم إزالة كتلته بمحلول بيبيريدين في DMF. تم بعد ذلك غسل الراتينج المزيل باستخدام DMF وغسله عدة مرات في وقت واحد باستخدام MeOH وDCM. تم غسل راتينج الاقتران مرة واحدة لمدة 3 دقائق تقريبًا باستخدام DMF (20 مل)، و3 مرات لمدة دقيقتين تقريبًا باستخدام الأيزوبروبانول (20 مل) و3 مرات باستخدام DCM (20 مل) لمدة دقيقتين تقريبًا في كل مرة. تم اختبار الربط بطريقة القيصر نينهيدرين.
تم ربط كل من الأحماض الأمينية المحمية التالية بالراتنج المغسول باستخدام DIC في DMF/DCM وتم إصداره كما هو موضح أعلاه بالتسلسل التالي: Fmoc-L-valine، Fmoc-L-lysine(Boc)، Fmoc-D-tryptophan، Fmoc-L-tyrosine (O-t-Bu) وFmoc-L-cysteine (Acm) (جميعها من Bachem California)، Boc-D-2-naphthylalanine (Synthethech، Albany، OR).
تمت إزالة انسداد سلسلة الببتيد المكتملة وحمايتها مرتين باستخدام 75:20:5 DCM/TFA/أنيسول (30 مل) لمدة دقيقتين تقريبًا وحوالي 25 دقيقة، وغسلها 3 مرات لمدة دقيقتين تقريبًا في كل مرة باستخدام DCM (20 مل)، أيزوبروبانول. (10 مل) وDCM (20 مل)، تم تحييدهما مرتين لمدة 5 دقائق تقريبًا مع 10% ثلاثي إيثيل أمين في DCM (20 مل) وغسلهما 3 مرات لمدة دقيقتين تقريبًا باستخدام DCM (20 مل) وMeOH (20 مل). تم تجفيف الراتنج تحت ضغط منخفض. وكان الوزن الجاف 3.91 جم (103% من المحصول النظري).
ب) H-D- -Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-NH 2
تم تعليق 2.93 جم من الراتنج المحمل بالببتيد من الخطوة (B) (1.3 مليمول مكافئ) في 50 مل من خليط MeOH/DMF 3:1. تم تبريد الملاط إلى درجة حرارة أقل من حوالي 10 درجات مئوية. تحت جو من النيتروجين وتم تطهير غاز الأمونيا الجاف حتى يتشبع المحلول به، بينما تم الحفاظ على درجة الحرارة أقل من حوالي 10 درجات مئوية. تم تقليب الملاط بلطف لمدة 24 ساعة تقريبًا، مما سمح لدرجة الحرارة بالارتفاع إلى حوالي 20 درجة مئوية. تم فحص درجة اكتمال التفاعل من خلال اختفاء وسيط إستر الميثيل باستخدام HPLC (مادة ماصة VYDAC®، حجم الحبوب 5 ميكرومتر، حجم المسام 100 Å، C18، الشطف تحت الظروف المتساوية 26% CH 3 CN في 0.1% TFA، السرعة 1 مل / دقيقة، التسجيل عند 220 مم، في ظل هذه الظروف، زمن التخلف Rt ~ 14 دقيقة لإستر الميثيل و~ 9.3 دقيقة لمنتج الأميد). تم تبريد خليط التفاعل وإضافة فائض من الأمونيا اللامائية حتى أصبحت مساحة الذروة المقابلة لإستر الميثيل في HPLC أقل من 10% من مساحة الذروة للمنتج المطلوب. تم تبريد الملاط إلى درجة حرارة أقل من 10 درجات مئوية تقريبًا، واستمر التحريك طوال الليل لترسيب الببتيد. تم فصل الراسب والراتنج بالترشيح وغسلهما بـ 15 مل من MeOH البارد. تم تجفيف الراسب والراتنج تحت ضغط مخفض، وتم استخلاص المنتج من الراتينج باستخدام محلول حمض أسيتيك مائي 50% (3 × 30 مل). أظهر تحليل HPLC وجود 870 مجم (0.70 مللي مول) من المنتج الرئيسي في الخليط (96% نقي في نظام HPLC الإيزوقراطي).
د) H-D- -Nal--Thr-NH 2
تم إذابة 500 مجم (0.40 مللي مول) من الببتيد من الخطوة (ب) في 300 مل من حمض الأسيتيك 4% وتم تسخينه إلى حوالي 55 درجة مئوية تحت النيتروجين. تم تقليب المحلول بسرعة وتم إضافة محلول 2% وزن/حجم من اليود في 7.7 مل من MeOH (0.60 مللي مول) في جزء واحد. تم تقليب الخليط لمدة 15 دقيقة تقريبًا، ثم تم إيقاف التفاعل بالمعايرة باستخدام محلول ثيوكبريتات الصوديوم 2% حتى يختفي اللون (~ 2 مل). تم تبريد الخليط إلى درجة حرارة الغرفةوتصفيتها. تمت تنقية الخليط بواسطة تحليل كروماتوجرافي تحضيري على عمود C8 (YMC، Inc.، Wilmington، NC) مع تدرج من الأسيتونيتريل في 0.1 مولار من أسيتات الأمونيوم، وتم تحليته على عمود C8 YMC مع تدرج من الأسيتونيتريل في 0.25 ن حمض أسيتيك، و مجفف بالتجميد ليعطي 350 ملجم من الببتيد المستهدف بنقاء 99%.
بناءً على الوصف أعلاه، يمكن لأي شخص ماهر في المجال التعرف بسهولة على السمات الأساسية للاختراع الحالي، ودون الخروج عن روحه ونطاقه، إجراء تغييرات وتعديلات مختلفة على الاختراع لتكييفه مع التطبيقات والظروف المختلفة. وبالتالي، فإن التجسيدات الأخرى للاختراع يتم تغطيتها أيضًا بواسطة المطالبات.
مطالبة
1. طريقة تحضير ببتيد الصيغة H-D--Nal-Thr-NH 2، الطريقة المذكورة تشتمل على الخطوات التالية:
(أ) ربط حمض أميني أول براتينج داعم صلب بواسطة رابطة أثير لتكوين "منتج اقتران أول"، والذي يتضمن (1) تفاعل محلول مائي من كربونات السيزيوم مع محلول كحولي للحمض الأميني الأول لتكوين الحمض الأميني الأول. ملح السيزيوم للحمض الأميني الأول، (2) الحصول على ملح السيزيوم الخالي من المذيبات للحمض الأميني الأول، (3) تفاعل راتينج الدعم الصلب مع ملح السيزيوم للحمض الأميني الأول في مذيب لابروتيكي قطبي لا مائي لتكوين "منتج الإضافة الأول"،
حيث الحمض الأميني الأول هو Boc-L-Thr، والذي يتوافق مع الحمض الأميني الطرفي C لهذا الببتيد، وراتنج الوسائط الصلبة عبارة عن راتنج من البوليسترين المكلور؛
(ب) إزالة حماية Boc من منتج الإضافة الأول باستخدام حمض لتكوين "منتج إضافة أول منزوع الحماية"؛
(ج) اختياريًا، إضافة إلى "منتج الارتباط الأول الذي تم إزالة حظره" "الحمض الأميني التالي"، والذي يتضمن تفاعل "الحمض الأميني التالي" مع "منتج المرفق الأول الذي تم إزالة حظره" في مذيب عضوي يحتوي على كاشف نمو الببتيد للحصول على "منتج الأحماض الأمينية التالي المحظور". إضافة"، حيث يحتوي "الحمض الأميني التالي" على مجموعة أمينية محجوبة من نوع Boc في السلسلة الرئيسية، وإذا كان هذا "الحمض الأميني التالي" يحتوي على مجموعة وظيفية واحدة أو أكثر في السلسلة الجانبية، إذن المجموعات الوظيفية في السلسلة الجانبية لا تحتاج إلى حماية أو أن هذه المجموعات الوظيفية في السلسلة الجانبية لديها مجموعات حماية مستقرة لعوامل إزالة الحماية الحمضية أو القلوية، على التوالي، Boc وFmoc؛
(د) إزالة حماية Boc من "المنتج التالي المحظور" والذي يتضمن تفاعل "المنتج التالي المحظور" مع حمض للحصول على "المنتج التالي المحظور"؛
(هـ) اختياريًا، تكرار الخطوتين (ج) و(د)، حيث تنتج كل دورة "منتجًا تم إلغاء حظره للمرفق التالي (X + 1)، حيث X هو عدد تكرارات الدورة المطلوبة؛
(هـ) إضافة "الحمض الأميني التالي" إلى "منتج الوصلة الأولى الذي تم رفع الحظر عنه" من الخطوة (ب) أو، اختياريًا، إلى "المنتج الذي تم رفع الحظر عنه للوصلة التالية (X+1)" من الخطوة (هـ)، والتي يتضمن إجراء تفاعل "الحمض الأميني التالي" مع "المنتج المفكك المحدد للملحق الأول" المحدد أو مع "المنتج المفكك المحدد للملحق التالي (X + 1)" في مذيب عضوي يحتوي على كاشف لتنمية الببتيد للحصول على "منتج المرفق التالي المحظور"، وهذا "الحمض الأميني التالي" يحتوي على مجموعة أمينية من السلسلة الرئيسية المحجوبة من Fmoc، بشرط أنه إذا كان "الحمض الأميني التالي" يحتوي على مجموعة وظيفية واحدة أو أكثر في السلسلة الجانبية، فإن المجموعات الوظيفية في السلسلة الجانبية لا تحتاج إلى حماية، أو أن المجموعات الوظيفية في السلسلة الجانبية لديها مجموعات حماية مقاومة للكواشف القلوية المستخدمة لإزالة حماية Fmoc؛
(ز) إزالة حماية "المنتج التالي المحظور" Fmoc، والذي يتضمن تفاعل "المنتج التالي المحظور" مع أمين أولي أو ثانوي لإنتاج "المنتج التالي المحظور"؛
(ح) اختياريًا، تكرار الخطوتين (هـ) و(ز)، مع إنتاج كل دورة "منتجًا محظورًا للمرفق التالي (X+1)، حيث X هو العدد المطلوب من تكرارات الدورة حتى يتم تضمينها في يتم إطلاق الببتيد والحمض الأميني قبل الأخير.
(1) إضافة حمض أميني طرفي N إلى "المنتج الذي تم إزالة حجبه من المدخل التالي (X+1)، والذي يتضمن تفاعل الحمض الأميني طرفي N مع "المنتج الذي تم إزالة حجبه من (X+1) التالي "الانضمام" في مذيب عضوي يحتوي على كاشف لتمديد الببتيد لتشكيل "منتج مرفق كامل محجوب" حيث يحتوي "الحمض الأميني N-terminal" على مجموعة أمينية أساسية محجوبة بواسطة Boc أو Fmoc؛
(ي) إزالة حماية Boc أو Fmoc من "المنتج المكتمل المحظور" الذي يشتمل على تفاعل "المنتج المكتمل المحظور" مع حمض في حالة Boc أو قاعدة في حالة Fmoc لتكوين منتج الببتيد المكتمل على الراتينج؛
(ي) إذا كان "منتج الببتيد المنتهي بالراتنج" يحتوي على مجموعات وظيفية ذات سلسلة جانبية، عندئذٍ يتم اختياريًا إزالة حماية المجموعات الوظيفية ذات السلسلة الجانبية "منتج الببتيد المنتهي بالراتنج"، والتي تتضمن تفاعل "منتج الببتيد المنتهي بالراتنج" مع كواشف إزالة الحماية المناسبة لإنتاج "منتج ببتيد كامل على راتينج منزوع الحماية"؛ و
(ك) شق الببتيد من حامل الراتينج الصلب لـ "منتج الببتيد النهائي على الراتنج" أو "منتج الببتيد النهائي على راتينج منزوع الحماية" للحصول على الببتيد، الذي يشتمل على تفاعل "منتج الببتيد النهائي على الراتنج" أو "منتج الببتيد النهائي على الراتنج" راتينج"؛ راتينج منزوع الحماية" مع الأمونيا، أو أمين أولي، أو أمين ثانوي حتى يكتمل انقسام الببتيد من الراتينج تقريبًا؛
بشرط تنفيذ الخطوتين (e) و(g) في تخليق الببتيد ست مرات بعد تكوين "منتج الارتباط الأول الذي تم إزالة الحظر عنه" بالصيغة H-L-Thr-resin، حيث يتم ربط الأحماض الأمينية اللاحقة بالترتيب: Fmoc-L-Cys(Acm)، Fmoc -L-Val، Fmoc-L-Lys(Boc)، Fmoc-D-Trp، Fmoc-L-Tyr(O-t-Bu) وFmoc-L-Cys (Acm) لتكوين H-Cys(Acm)-Tyr (O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-الراتنج.
2. الطريقة طبقاً للمطالبة 1، حيث تكون الأمونيا، الأمين الأولي أو الأمين الثانوي في الخطوة (ك) في مذيب يحتوي على كحول واختيارياً مذيب قطبي لابروتيكي.
3. الطريقة حسب المطالبة 1، حيث تشتمل الخطوة (ل) أيضًا على الخطوات التالية:
(ط) يعجل الببتيد المشقوق من المذيب؛
(2) تصفية دعم الراتنج الصلب والببتيد المترسب، و
(ثالثا) استخراج الببتيد بمحلول حمضي لعزل الببتيد.
4. الطريقة وفقًا لأي من المطالبات من 1 إلى 3، حيث يكون الحمض الأميني الأول هو ملح السيزيوم لـ Boc-L-Thr، مما ينتج عنه راتنج Boc-L-Thr كمنتج الاقتران الأول، و"منتج الاقتران الأول المزيل للحجب" "هو H-L-Thr -الراتنج.
5. الطريقة وفقًا للمطالبة 4، حيث يكون الحمض المستخدم لإزالة مجموعة الحماية Boc في الخطوة (i) هو حمض ثلاثي فلورو أسيتيك (TFA).
6. الطريقة وفقًا للمطالبة 5، حيث يكون المذيب العضوي هو كلوريد الميثيلين، أو الكلوروفورم، أو ثنائي ميثيل فورماميد، وكاشف نمو الببتيد هو ثنائي إيزوبروبيل كاربوديميد، أو ثنائي سيكلوهيكسيل كاربوديميد، أو N- إيثيل - ن "- (3- ثنائي ميثيل - أمينوبروبيل) كاربودي إيميد.
7. الطريقة وفقًا للمطالبة 6، تتضمن ربط Boc-D--Nal بـ H-Cys(Acm)-Tyr(O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-resin وفقا للخطوة (ط) للحصول على Boc-D--Nal-Cys(Acm)-Tyr(O-t-Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-الراتنج.
8. الطريقة وفقًا للمطالبة 7، والتي تشتمل على الإزالة المتزامنة لمجموعة Boc التي تحجب D- -Nal، ومجموعة O-t-Bu التي تحمي Tyr، ومجموعة Boc التي تحمي Lys في Boc-D- -Nal-Cys(Acm)- Tyr(O-t -Bu)-D-Trp-Lys(Boc)-Val-Cys(Acm)-Thr-راتنج، وفقًا للخطوة (د) للحصول على منتج الببتيد المكتمل على راتينج الصيغة H-D--Nal-Cys (Acm)-Tyr-D -Trp-Lys-Val-Cys(Acm)-Thr-الراتنج.
9. الطريقة وفقًا للمطالبة 8، تشتمل على شق الببتيد H-D--Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr من الراتنج الصلب عن طريق تنفيذ التفاعل H-D- -Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-راتنج مع الأمونيا في مذيب يحتوي على كحول واختياريًا مذيب قطبي لابروتيكي حتى يتم التخلص منه بشكل كامل لإعطاء H-D--Nal -Cys (Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-NH 2 .
10. العملية طبقاً للمطالبة 9، حيث يكون الكحول ميثانول والمذيب اللابروتيكي القطبي هو ثنائي ميثيل فورماميد.
11. الطريقة وفقًا للمطالبة 10، تتضمن في نفس الوقت إزالة مجموعات Acm التي تحمي Cys وإعادة تدوير بقايا Cys الناتجة غير المحمية في "منتج الببتيد الكامل على الراتينج" بالصيغة H-D--Nal-Cys(Acm)-Tyr-D -Trp- Lys-Val-Cys(Acm)-Thr-NH 2 عن طريق تنفيذ تفاعل H-D- -Nal-Cys(Acm)-Tyr-D-Trp-Lys-Val-Cys(Acm)-Thr-NH 2 بمحلول اليود في الكحول لإكمال عملية إزالة الحماية والتدوير بشكل كبير لإعطاء H-D--Nal-Thr-NH 2 .